| 🎓 Заказ №: 22226 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Дайте обоснование видоизмененному методу Къельдаля для количествен-ного определения ЛС. Приведите примеры, напишите химизм, выведите молярные массы эквивалентов.
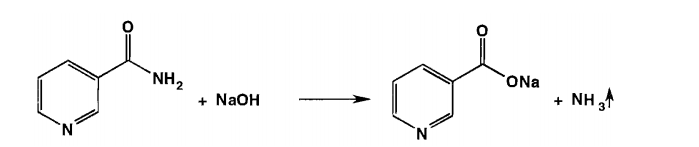
Решение: Метод Кьельдаля — метод количественного определения азота в органических соединениях. Различают три варианта метода Къельдаля: классический метод Къельдаля, микрометод Къельдаля, видоизмененный метод Къельдаля. Видоизмененный метод Къельдаля основан на гидролитическом разложении ЛС в присутствии натрия гидроксида, поглощении образующегося аммиака раствором кислоты борной, и титровании мета- и тетраборатов аммония раствором хлористоводородной кислоты. Количественное определение никотинамида

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- При окислении 10 г алюминия выделится 309,6 кДж теплоты.
- Написать в молекулярной форме уравнения реакций, которые выражаются следующими ионными уравнениями: а) 2 3 3 2 3 3 Bi CO Bi (CO ) ; б) 2 3 2 SiO3 2H H SiO ; в) 3 4 2
- В газофазной реакции N2 + Н2 ↔ NН3 начальные концентрации азота и водорода составляли 6 и 11,2 моль/л, соответственно.
- Соотнесите мольное отношение «ЛС : титрант» с молярной массой эквив алента (приведите химизм метода, дайте обоснование, выберите молярную массу эквивалента)
- Среди перечисленных ниже солей укажите те, которые подвергаются гидролизу: KNO3, Cr2(SO4)3, AlI3, CaCl2, K2SiO3.
- Определить объем углекислого газа при температуре 20ºС и давлении 1,12 атм., который можно получить при сжигании 5 т угля, содержащего 95 % углерода.
- Относительная плотность галогеноводорода по воздуху 2,8.
- В реакторе объемом 100 л смешали 7 молей метана и 5 молей паров воды.
- Чем измеряется скорость химических реакций ?
- Составить уравнение окислительно-восстановительной реакции с использованием метода электронного баланса; рассчитать массу восстановителя, необходимую для взаимодействия с окислителем, объемом V и концентрацией С.
