| 🎓 Заказ №: 22215 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Обоснуйте испытание лидокаина гидрохлорида по показателю «Растворимость» (в спирте 96 %) в соответствии с требованиями ФС.2.1.0123.18 (Приложения № 3, 4).
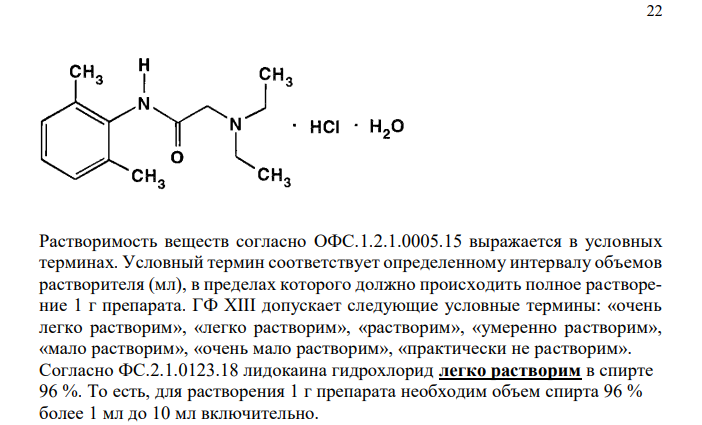
Решение Лидокаина гидрохлорид, Lidocaine Hydrochloride 22 Растворимость веществ согласно ОФС.1.2.1.0005.15 выражается в условных терминах. Условный термин соответствует определенному интервалу объемов растворителя (мл), в пределах которого должно происходить полное растворение 1 г препарата. ГФ XIII допускает следующие условные термины: «очень легко растворим», «легко растворим», «растворим», «умеренно растворим», «мало растворим», «очень мало растворим», «практически не растворим». Согласно ФС.2.1.0123.18 лидокаина гидрохлорид легко растворим в спирте 96 %. То есть, для растворения 1 г препарата необходим объем спирта 96 % более 1 мл до 10 мл включительно.

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Приведите расчет интервала навески соли (М.м. калия бромида 119,00) исходя из чувствительности иона (И.м. иона калия 39,01) для доказательства подлинности калия бромида по катиону калия по методике А (Приложение № 2).
- Между какими веществами: серная кислота (конц.), оксид железа(III), соляная кислота, алюминий, хлорид цинка, вода — возможны химические реакции?
- Железо покрыто оловом. Составьте схему процессов на электродах во влажном воздухе (pH ≈ 7): а) A (Sn): Sn0 -2ē→Sn2+; K (Fe): 2H++2ē→H2 0 б) A (Fe): Fe0 -2ē→Fe2+; K (Sn): 2H++2ē→H2 0 в) A (Sn): Sn0 -2ē→Sn2+; K (Fe): O2+2H2O+4ē→4OHг) A (Fe): Fe0 -2ē→Fe2+; K (Sn): O2+2H2O+4ē→4OH
- Вычислите электродный потенциал металла (Me Me E n), находящегося в растворах солей. Металл — Cr
- Дайте заключение о качестве субстанции натрия тетрабората по количественному содержанию, если при ацидиметрическом определении по методике ФС.2.2.0012.15 (Приложение № 3) на навеску субстанции 0,4980 г израсходовалось 26,50 мл 0,1 М раствора хлористоводородной кислоты (К = 0,9978).
- Для атома некоторого элемента возможны четыре состояния, записанные в виде электронных формул: 1s 22s 22p 63s 23p 5 ; 1s 22s 22p 63s 23p 43d 1 ; 1s 22s 22p 63s 23p 33d 2 ; 1s 22s 22p 63s 13p 33d 3 .
- Вычислите 500 H , S , G реакции 3 2 3 . Fe2O3(к) H2 Fe(к) H2O
- Вычислите стандартные изменения (при 298 К) энтальпии, энтропии и свободной энергии Гиббса. По данным 2NO(г) + Br2(г) = 2NOBr(г)
- Какая из предложенных солей CuSO4, Na2S гидролизуется по аниону.
- Дайте обоснованный ответ, в каком направлении может самопроизвольно протекать заданная реакция? Cu + HgCl2 ⇆ CuCl2 + Hg
