| 🎓 Заказ №: 22228 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Применение правила фаз и правила рычага к диаграмме плавкости (приведите несколько примеров).
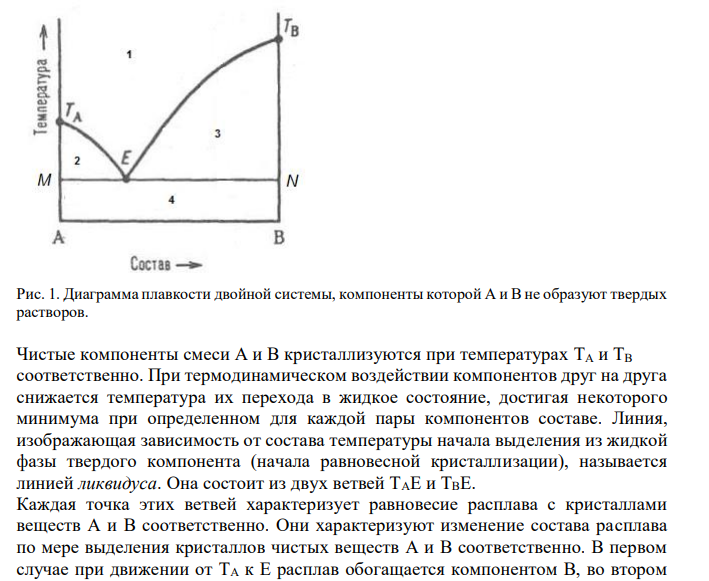
Решение: Простейший вариант диаграммы плавкости соответствует случаю, когда компоненты А и В образуют одну жидкую фазу (расплав или раствор), при охлаждении которой только выделяются (кристаллизуются) индивидуальные вещества (не образуются ни твердые растворы, ни химические соединения). Окисление Fe2+ Окисление C6H6 244 Рис. 1. Диаграмма плавкости двойной системы, компоненты которой А и В не образуют твердых растворов. Чистые компоненты смеси А и В кристаллизуются при температурах TА и TВ соответственно. При термодинамическом воздействии компонентов друг на друга снижается температура их перехода в жидкое состояние, достигая некоторого минимума при определенном для каждой пары компонентов составе. Линия, изображающая зависимость от состава температуры начала выделения из жидкой фазы твердого компонента (начала равновесной кристаллизации), называется линией ликвидуса. Она состоит из двух ветвей ТАЕ и ТВЕ. Каждая точка этих ветвей характеризует равновесие расплава с кристаллами веществ А и В соответственно. Они характеризуют изменение состава расплава по мере выделения кристаллов чистых веществ А и В соответственно. В первом случае при движении от TA к Е расплав обогащается компонентом В, во втором при движении от TB к Е – компонентом А. Точка Е (эвтектическая точка) пересечения ветвей ТАЕ и ТВЕ показывает температуру и состав расплава, который находится в равновесии как с кристаллами вещества А, так и с кристаллами вещества В. Линия MN, изображающая зависимость от состава температуры окончания равновесной кристаллизации при охлаждении (или начала плавления при нагревании), называется линией солидуса. Линии ликвидуса и солидуса делят все поле на отдельные области. В области 1 существует одна жидкая фаза, в состав которой входят два компонента. Число степеней свободы в этой области равно: С = К – Ф + 1 = 2 – 1+ 1 = 2, то есть система является двухвариантной. Это значит, что в области 1 можно в определенных пределах произвольно изменять и температуру, и состав, не изменяя число фаз. В областях 2 и 3 существуют две фазы: кристаллические вещества А и В соответственно и расплав (жидкий насыщенный раствор). В обеих областях число степеней свободы равно: С = К — Ф + 1 = 2 — 2 + 1 = 1, то есть, в обоих случаях системы являются одновариантными. Это значит, что можно произвольно изменять либо температуру, либо состав.


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Сопряженные реакции.
- Во сколько раз увеличится скорость химической реакции, если увеличится температура на 40°С, а температурный коэффициент равен 3,75?
- Какой объем оксида углерода (IV) при н.у. вступает в реакцию с гидроксидом калия массой 22,4 г?
- Построение изотермы адсорбции по изотерме поверхностного натяжения.
- Окислительно-восстановительные реакции протекают по приведенным схемам. Gе + HNO3 → H2GeO3 + NO2 + H2O
- Какое количество вещества соли получится, если 6,5г цинка «растворить» в 200 г 40 %-ного раствора серной кислоты.
- Какую массу 28 %-ного раствора гидроксида калия надо взять для реакции с раствором сульфата меди (II), чтобы получить гидроксид меди (II) количеством вещества 0,2 моль?
- Определение величины ζ-потенциала по скорости электрофореза.
- Какое количество вещества содержится в образце 9,8 г гидроксида натрия.
- Коллоидная защита. Механизм защитного действия.
