| 🎓 Заказ №: 22219 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Рассчитайте объем 0,02 М раствора натрия гидроксида, который израсходуется на совместное титрование ингредиентов лекарственной смеси: Эфедрина гидрохлорида 0,6 Раствора новокаина 1%-200 мл, если на определение взят 1 мл раствора (М.м.: эфедрина гидрохлорида 201,70; новокаина 272,78). Приведите обоснование метода и соответствующие уравнения реакций.
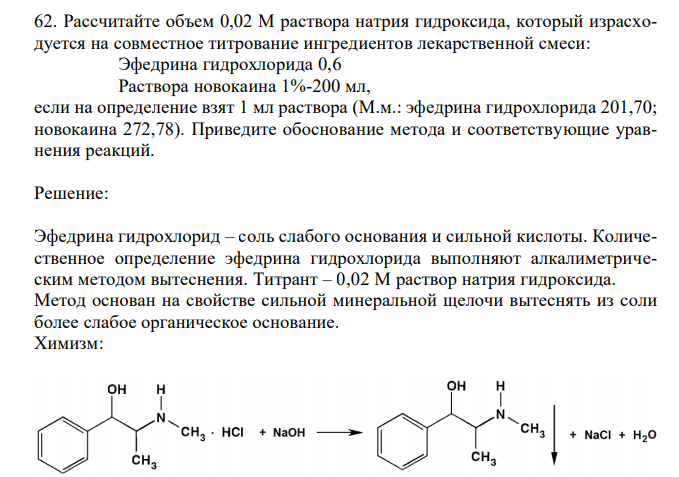
Решение: Эфедрина гидрохлорид – соль слабого основания и сильной кислоты. Количественное определение эфедрина гидрохлорида выполняют алкалиметрическим методом вытеснения. Титрант – 0,02 М раствор натрия гидроксида. Метод основан на свойстве сильной минеральной щелочи вытеснять из соли более слабое органическое основание. Химизм: Коэффициент стехиометричности Kстех 1 Расчет титра Т М м K М мг мл эф стех . . 201,7010,02 4,034 / Формула расчета объема раствора титранта 172 T m V 1000 где: V объем раствора титранта, пошедший на титрование, мл; mмасса вещества в навеске, г; Т титр определяемого вещества, мг/мл. Масса эфедрина гидрохлорида в навеске г P m а mэф 0,003 200 0,6 1 где: a – навеска лекарственной формы, мл; P – объем лекарственной формы, мл. Количественное определение новокаина выполняют алкалиметрическим методом. Титрант – 0,02 М раствор натрия гидроксида. Метод основан на нейтрализации связанной кислоты хлористоводородной раствором основания.


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- В каком количестве воды следует растворить 30 г KBr для получения 6 % раствора?
- При сгорании 11,5 г жидкого этилового спирта выделилось 308,71 кДж теплоты
- На основании стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ вычислите G 298 реакции, протекающей по уравнению: СО2(г) + 4Н2(г) = СН4(г) + 2Н2О(ж) Возможна ли эта реакция при стандартных условиях?
- Вычислите молярную концентрацию эквивалента карбоната натрия с массовой долей Na2CO3 16 % плотностью 1,170 г/мл.
- Какое количество электричества в кулонах и ампер часах потребуется для полного выделения никеля из раствора, содержащего его сульфат массой 30,9 г.
- На основании стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ вычислите G о 298 реакции, протекающей по уравнению: 4NН3(г) + 5О2(г) = 4NО(г) + 6Н2О(г)
- Потенциал электрода Pt, H2/раствор HCl неизвестной концентрации равен – 118 мв.
- Восстановление Fe3O4 оксидом углерода идет по уравнению: Fe3О4(к) + СО(г) = 3FeO(к) + СО2(г) Вычислите G 298 и сделайте вывод о возможности самопроизвольного протекания этой реакции при стандартных условиях
- Составьте молекулярные и ионные уравнения реакций взаимодействия в растворах между: H2 SO4 и NaOH.
- Как изменится скорость прямой реакции 2NO(г.) + O2(г.) = 2NO2(г.) при уменьшении объема в 2 раза?
