| 🎓 Заказ №: 22180 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Схема химико-токсикологического исследования формальдегида.
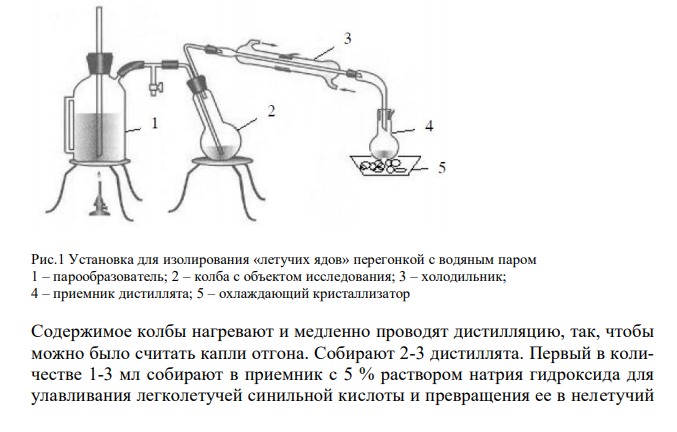
Формальдегид Основные физические и химические свойства Формальдегид – бесцветный газ с резким специфическим запахом, хорошо растворимый в воде, спиртах и полярных растворителях. При температуре ниже 10 °С формальдегид легко полимеризуется и образует полимер параформальдегид или параформ. Из-за низкой электронной плотности на атоме углерода формальдегид легко вступает в реакции даже со слабыми нуклеофилами. Этим, в частности, объясняется тот факт, что в водных растворах формальдегид находится в гидратированной форме. Формальдегид вступает во все реакции, характерные для алифатических альдегидов. В частности, в реакции с нуклеофилами и восстановительными реагентами. Метаболизм 212 Формальдегид выводится из организма частично в неизменном виде. Основная часть его окисляется до муравьиной кислоты, а затем до оксида углерода (IV). Изолирование Формальдегид легко испаряется, поэтому для его изолирования применяют метод перегонки с водяным паром. Наиболее важными объектами для судебно-химической экспертизы служат моча, почки, печень, сердце, кровь. Объект в количестве 100 г помещают в круглодонную колбу таким образом, чтобы она заполнилась не более чем на 1/3 её объема, подкисляют до рН 2-3. Для подкисления используют щавелевую или виннокаменную кислоту, а не минеральные кислоты, так как первые не гидролизуют такие вещества, как синильная кислота или сернокислый эфир фенолов. В результате гидролиза при неправильном ведении анализа возможно загрязнение дистиллята дополнительными примесями. Собирают прибор для перегонки с водяным паром, который состоит из герметично соединенных друг с другом парообразователя, колбы с объектом исследования, холодильника и приемника. Рис.1 Установка для изолирования «летучих ядов» перегонкой с водяным паром 1 – парообразователь; 2 – колба с объектом исследования; 3 – холодильник; 4 – приемник дистиллята; 5 – охлаждающий кристаллизатор Содержимое колбы нагревают и медленно проводят дистилляцию, так, чтобы можно было считать капли отгона. Собирают 2-3 дистиллята. Первый в количестве 1-3 мл собирают в приемник с 5 % раствором натрия гидроксида для улавливания легколетучей синильной кислоты и превращения ее в нелетучий


| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- На основании стандартных энтальпий образования и стандартных энтропий соответствующих веществ вычислите изменение энергии Гиббса реакции, протекающей по уравнению С2Н4(г) + 3О2(г) = 2СО2 (г) + 2Н2О(ж).
- Как называют полимер состава
- Составьте схему гальванического элемента, состоящего из двух алюминиевых пластинок, опущенных в растворы его соли с концентрацией [Al3+] = 1 моль/л у одного электрода и [Al3+ ] = 0,1 моль/л у другого электрода. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
- На р-подуровне находятся 3 электрона. Как они располагаются на р-орбиталях в нормальном состоянии?
- Напишите электронные и электронно-графические формулы атомов элементов с порядковыми номерами 5, 20, 43.
- Металл – Ве. По реакции гидроксида этого металла с ортофосфорной кислотой получите кислую соль. Степень окисления Ве соответствует номеру группы этого металла в периодической таблице.
- Чему равен температурный коэффициент скорости реакции, если при понижении температуры на 30°, время протекания реакции увеличилось в 64 раза?
- Какой металл целесообразней выбрать для протекторной защиты от коррозии свинцовой оболочки кабеля: цинк, магний или хром? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии. Каков состав продуктов коррозии?
- Кусок латуни обработали азотной кислотой. Раствор разделили на две части. К одной из них прибавили избыток раствора аммиака, к другой – избыток раствора щелочи. Какие соединения цинка и меди образуются при этом? Составьте уравнения соответствующих реакций.
- Кондуктометрическое титрование. Приведите примеры кондуктометрического титрования: а) сильной кислоты сильным основанием; б) смеси слабой и сильной кислот сильным основанием; приведите кривые титрования и объясните их ход.
