| 🎓 Заказ №: 22204 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Что такое гибридизация валентных орбиталей. Какое строение имеют молекулы типа ABn, если связь в них образуется за счет sp-, sp2 -, sp3 — гибридизации орбиталей атома А? Приведите примеры молекул с указанными типами гибридизации.
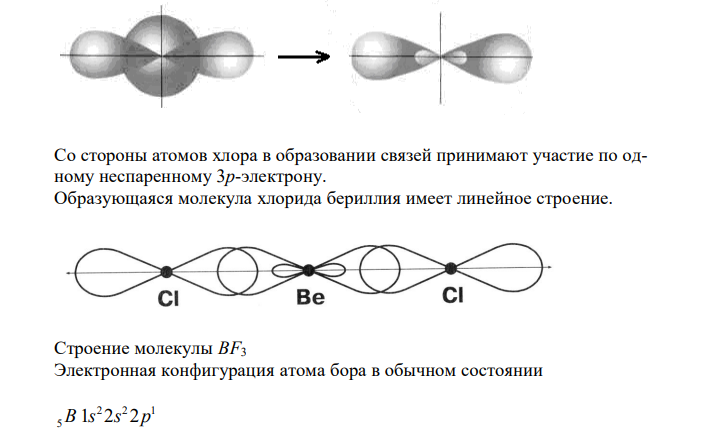
Решение: Гибридизация – гипотетический процесс смешения разных (s, p, d, f) орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим характеристикам. Молекулы, в которых связь образуется за счет sp-гибридизации орбиталей центрального атома, имеют линейное строение. Молекулы, в которых связь образуется за счет sp2 -гибридизации орбиталей центрального атома, имеют треугольное строение. Молекулы, в которых связь образуется за счет sp3 -гибридизации орбиталей центрального атома, имеют тетраэдрическое строение. Строение молекулы BeCl2 Электронная конфигурация атома бериллия в обычном (основном) состоянии 2 2 Be 1s 2s Перед образованием связей атом бериллия переходит в возбужденное состояние, один из 2s-электронов атом бериллия перескакивает на 2p-орбиталь. Таким образом, у атома бериллия появляются два неспаренных электрона. Далее электронные плотности s- и p-орбиталей неспаренных электронов атома бериллия смешиваются (усредняются по энергии). В результате этого процесса (sp-гибридизации) получаются две одинаковые гибридные sp-орбитали, расположенные в пространстве под углом 180º друг к другу. Со стороны атомов хлора в образовании связей принимают участие по одному неспаренному 3p-электрону. Образующаяся молекула хлорида бериллия имеет линейное строение. Строение молекулы BF3 Электронная конфигурация атома бора в обычном состоянии 2 2 1 5B 1s 2s 2p



| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Какие четыре квантовых числа характеризуют состояния электронов в атоме?
- 2 мл 96%-й серной кислоты (плотность 1,84 г/см3 ) разбавили до 3 л. вычислите рН раствора при α = 1.
- Какой должна быть концентрация ионов [Zn2+] в полуячейке, чтобы пара Zn/Zn2+ при T = 298 К имела электронный потенциал -0,819 В?
- Определите, чему равен заряд комплексных ионов [Cr(NH3)5NO3]; [Pd(NH3)Cl3], [Ni(CN)4], если комплексообразователями являются Сr 3+ , Pd2+ , Ni2+
- Изотоп кремния-30 образуется при бомбардировке — частицами ядер атомов алюминия-27. Составьте уравнение этой ядерной реакции и запишите его в сокращенной форме.
- Расставьте коэффициенты в уравнении реакции методом электронного баланса: HNO2 + HCl + KMnO4 → KNO3 + Mn(NO3)3 + H2O + KCl
- Определить степень диссоциации и концентрацию ионов [OH– ] в 0,01Н растворе NH4OH, если КД = 5 2 10 .
- Определите заряд следующих комплексных ионов: [Cr(NH3)5NO3], [Pt(NH3)Cl3], [Ni(CN)4], если комплексообразователями являются Cr3+, Pt2+, Ni2+.
- Составить уравнение электродных реакций, протекающих при электролизе с нерастворимыми анодами расплавов и водных растворов SnSO4, MnCl2.
- Составьте координационные формулы следующих комплексных соединений кобальта: 3NaNO2·Co(NO2)3, CoCl3·3NН3·2Н2О, 2KNO2·NH3·Co(NO2)3
