| 🎓 Заказ №: 22189 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
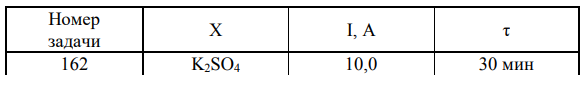
Электролиз водного раствора вещества X проводили с угольными электродами катодного и анодного процессов. Вычислите массы веществ, выделившихся на катоде и на аноде. Определите объем выделившихся газообразных веществ (н.у.).
Решение: Уравнения электродных процессов: На аноде выделяется газообразный кислород, в прианодном пространстве образуется серная кислота. На катоде выделяется газообразный водород, в прикатодном пространстве образуется гидроксид калия. Согласно закону Фарадея масса вещества, выделившегося на электроде, находится по формуле

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Как изменится скорость реакции, если увеличить давление системы 2S (ТВ) + 3O2 (Г) = 2SO3(Г) в 3 раза.
- Надо получить 100 г свинцо-оловянного сплава, содержащего 60 % свинца и 40 % олова.
- Составьте схему гальванического элемента, образованного двумя данными металлами, погруженными в растворы солей с известной активностью ионов; рассчитайте ЭДС этого элемента и G298 .
- Окислительно-восстановительные реакции протекают по приведенным схемам. K2Cr2O7 + KBr + H2SO4 → Cr2(SO4)3 + Br2 + K2SO4 + H2O
- В каком направлении будут перемещаться электроны во внешней цепи следующих гальванических элементов а) Mg | Mg2+ | | Pb2+ | Pb б) Pb | Pb2+| |Cu2+ | Cu в) Cu | Cu2+| | Ag2+| Ag
- К 500 г 30 % масс. раствора аммиака (d20 4 раствора = 1,09 г/мл) добавили 1л воды.
- Определить возможность самопроизвольного протекания прямой реакции при стандартных условиях 3Fe(TB) + 4H2O(Г) = Fe3O4(TB) + 4H2(Г).
- Напишите уравнения анодного и катодного процессов, суммарные ионномолекулярное и молекулярное уравнения этих процессов, протекающих в гальваническом элементе. Bi | Bi(NO3)3 || Cu(NO3)2 | Cu
- На основании стандартных энтальпий образования H f ,298 и абсолютных стандартных энтропий соответствующих веществ S298 вычислите G298 реакции 4NH3(г) 5О2(г) 4NO(г) 6H2О(г) и сделайте вывод о возможности самопроизвольного протекания этой реакции в стандарнтных условиях.
- Вычислите константу равновесия прямой реакции N2О4 2NО2, если равновесная концентрация NО2 равна 0,28 моль/л, а равновесная концентрация N2О4 = 0,30 моль/л.
