Оглавление:

Метод валентных связей
- Метод валентной связи. BC метод Химическая связь образуется двумя неспаренными электронами Антипараллельное вращение. В этом случае обобщение Появление электронов, т. Е. Образуются электронные пары, Лежа на двух атомах. В 1927 году немецкие ученые В. Гейтлер и Ф. Лондон Квантово-механический расчет взаимодействия атомов водорода.
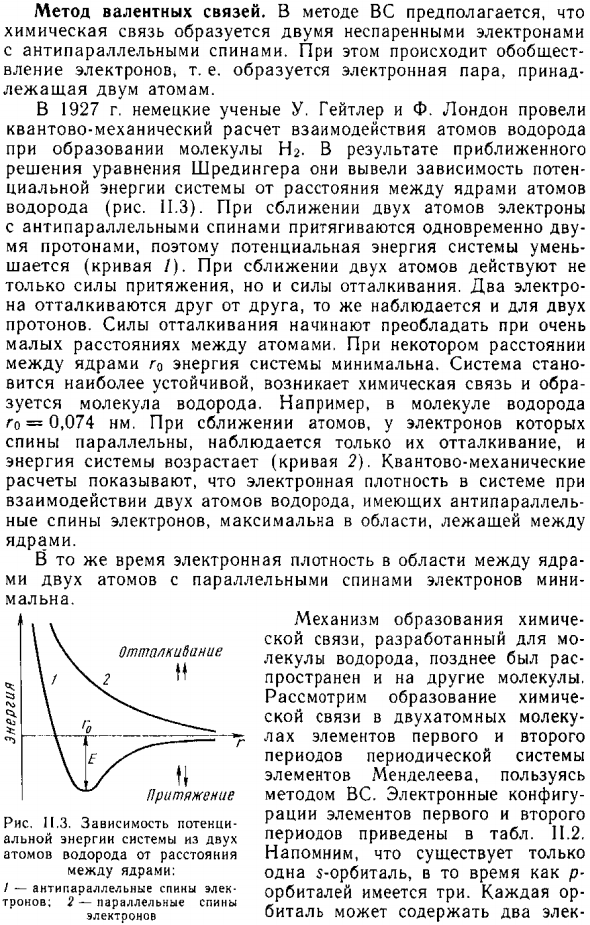
- При образовании молекул ртути — как результат приближения. Решение Шредингера получило потенциальную зависимость Социальная энергия системы на расстоянии между ядрами Водород (рис. 11.3). Когда два атома становятся ближе друг к другу, электрон В антипараллельных спинах два притягиваются одновременно Протоны, а значит и потенциальная энергия системы снижается Это будет решено (кривая /).
Когда два атома собираются вместе, они не работают Не только сила притяжения, но и сила отталкивания. Людмила Фирмаль
2 электро Не отталкивайтесь друг от друга, то же самое наблюдается для двух Протон. Отвращение начинает становиться очень доминирующим Небольшое расстояние между атомами. На расстоянии Между движущимися ядрами энергия системы минимальна. Система Стано Наиболее устойчивые, химические связи происходят, Молекулы водорода образуются. Например, молекула водорода Go = 0,074 нм.
Когда атомы приближаются друг к другу, их электроны Спина параллельна и наблюдается только отталкивание. Увеличивает энергию системы (кривая 2). Квантовая механика Рассчитайте электронную плотность системы Антипараллельное взаимодействие с двумя атомами водорода Максимум спина электрона в области между Ядро. В то же время электронная плотность в межъядерной области Ми двух атомов с параллельным спином электрона Maruna.
- Механизм химического образования Предназначен для общения. Молекула водорода, позднее rac Распространяется на другие молекулы, Рассмотрим образование химических веществ Связь двухатомных молекул Лах первого и второго элементов Период циклической системы Менделеевские элементы и утилизация Солнечный метод. Электронная конфигурация Первый и второй элемент трансивера Период указан в таблице. 11.2.
Помните, что есть только Одна 5 орбита, р- Есть три орбиты. И.З. Потенциальная зависимость Полная энергия двух систем Атом водорода на расстоянии Между ядрами: / -Anti-Parallel Back Elec Трон; 2-х параллельная спина электрон Таблица 11.2. Электронная конфигурация элементов в первом и втором периодах Строение и строение двухатомных молекул методом Эльмас Масио rnd- но высокая но контрмера электрон.
Все операции Два электрика для битвы оттаивание очарование Rns. Людмила Фирмаль
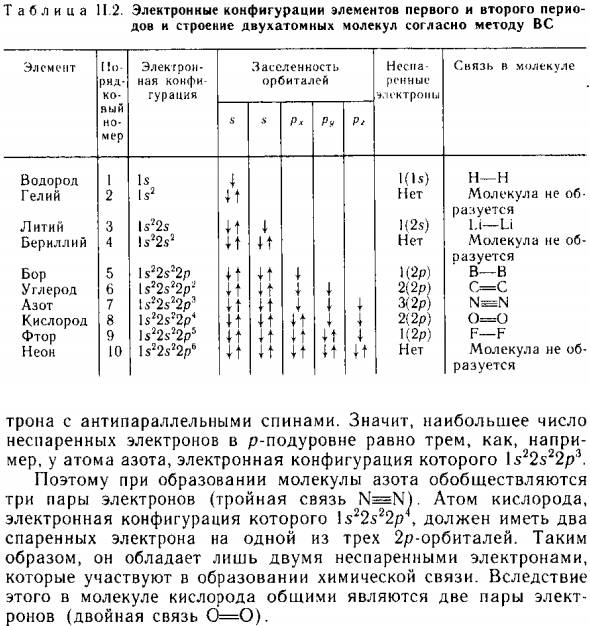
Нах Конфи Дозирование население Orbit Nesuga Ронни ^ .к’ктрома Принц молекул X .4 Rx Rya Rg Водород 1 15 1 1 (1 ..} N-N Нет геля и 2 15 ^ и М молекул ра: 1 Литий 3 15 ‘^ 25 И \ 1 (25) 1. 1-ы Молекулы бериллия 4 ls ^ 2 s ^ u и No M Для развития Бор 5 15 ^ 25 ^ 2рии1 (2р) В-В Углерод 6 \ 5 ^ 25 ^ 2р ^ ии \ 2 (2р) с = с Азот 7 л 6 • ^ 2 с ^ 2 р ‘и 3 (2р) N = N Кислород 8 15 ^ 25 ^ и вы и 2 (2р) 0 = 0 Фтор 9 лс ^ 2 с ^ 2 р ^ и ты и ты \ (2р) р-р Неон 10 15 ^ 25 ^ и а и нет М молекула не о Для развития Трон с антипараллельным вращением.
Поэтому максимальное количество Например, p подуровня неспаренных электронов равны 3. Например, атом азота, чья электронная конфигурация \ 5 ^ 28 ^ 2р ^. Поэтому социализация при образовании молекул азота 3 набора электронов (тройная связь, атом кислорода.
Есть две электронные конфигурации Соедините электроны на одной из трех 2p-орбиталей. Следовательно, существует только два неспаренных электрона. Участвует в образовании химических связей. для Две кислородные пары являются общими в этой молекуле кислорода роны (двойная связь 0 = 0).
Смотрите также:
| Полярность связи | Валентность |
| Ионная связь | Донорно-акцепторный механизм образования ковалентной связи |
Если вам потребуется помощь по химии вы всегда можете написать мне в whatsapp.
