Оглавление:





Параметры состояния воды и водяного пара
- Из-за незначительной сжимаемости воды можно предположить, что плотность воды при 0°С и при любом давлении постоянна, но = 0,001 М ’ / ка. Точка отсчета для внутренней энергии энтальпий и энтропии берется из ОС и соответствующего давления насыщения P = = 0.00610 бар. Если использовать эти параметры, то энтальпия, энтропия и внутренняя энергия воды также будут условно равны нулю: а= 0 ’= 0’ а = 0. В процессе нагрева воды она нагревается до температуры кипения, и удельный объем воды при температуре кипения»больше объема О. Соответствующие значения о для воды в зависимости от температуры и давления состояния на нижней граничной кривой или на левой ее стороне описаны в литературе.
Количество тепла (p = sop), которое необходимо сообщить воде, чтобы нагреть воду от 0°C до температуры кипения процесса, называется теплом жидкости. Это количество тепла определяется по формуле (9.15 утра)) Где СРА-средняя теплоемкость воды в диапазоне температур 0°С-С. При низких температурах по сравнению с TI можно считать, что C, в= 4,1865 кДж / кг-град.
Помимо указанных сил, в реальных жидкостях и газах действуют также другие силы, существование которых обусловливается вязкостью. Людмила Фирмаль
Мы используем первый закон термодинамики в изобарном процессе нагрева воды / =И ’ — » о + (9.17)) Здесь и ’ — это внутренняя энергия воды в Точке кипения. При 0°C ’ ₁ = 0 происходит расширение жидкости / ’=₽( «’-)(9.18) При высоком давлении значения только существенно заметны, а q-К и ’. (9.19) Энтальпия воды при температуре кипения определяется по общей формуле «А + д» — (9.20)) предполагая ’= и ’+ po ’»= 0″, вы получаете»I» =и» = d». (9.21) В процессе нагрева жидкости от 0°С до температуры кипения ее энтропия возрастает. Это и есть формула Д’»=«- (9.22) пиар( 0 и КПВ = 4,1865 кДж / (кг град).
Как уже говорилось, в экспериментах было установлено, что в процессе испарения жидкость, нагретая до температуры кипения при этой температуре и определенном давлении, превращается в пар. Р = const! Для того чтобы преобразовать 1 кг воды при температуре кипения в сухой насыщенный пар при той же температуре、 Теплота r называется скрытой теплотой испарения. Согласно первому закону термодинамики р = п — _ А ’ + Р, (9.24) Вот внутренняя энергия „сухого насыщенного пара“.» / * — Работа расширения в процессе испарения.
Разность между внутренней энергией и»- » и «затраченной на работу над внутренними силами» называется внутренней теплотой образования пор, обозначаемой буквой R. теплота, затраченная на работу над внешними силами Я ’= П(В-В) (9.25) И называется внешним теплом испарения. Покажите это в гривне, и поэтому р = п + ф — (9.2 с) За счет того, что процесс испарения происходит при постоянном давлении.
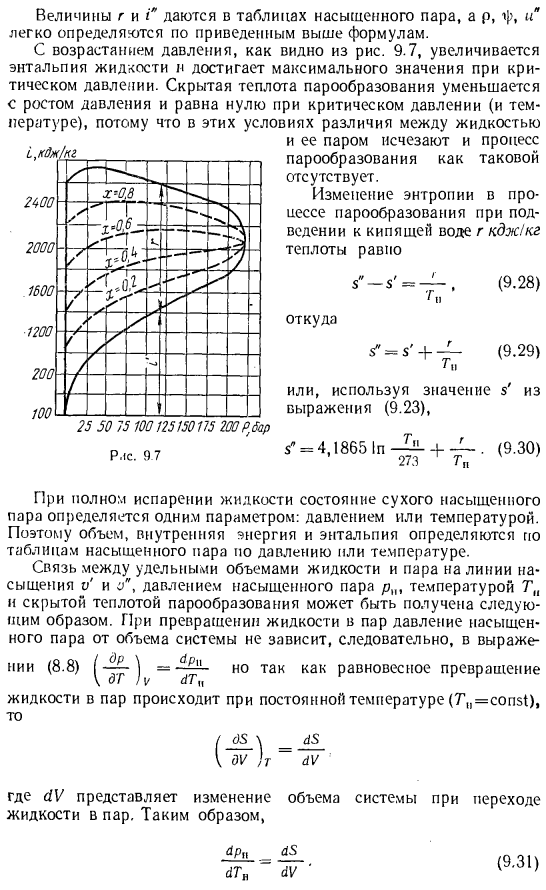
- Значения r и 1, приведены в таблице насыщенного пара, а p, m/>, и легко определяются по приведенной выше формуле. Как видно из рисунка, когда давление повышается9. 7, энтальпия жидкости увеличивается, и с критическим давлением она достигает максимального значения. Скрытая теплота испарения уменьшается с увеличением давления и становится равной нулю при критическом давлении(и температуре).В этих условиях разница между жидкостями Когда жидкость полностью испаряется, состояние сухого насыщенного пара определяется 1 параметром-давлением или temperature. So, объем, внутренняя энергия, энтальпия определяются из таблицы насыщенного пара при давлении или температуре.
Соотношение между удельным объемом жидкости и паром на линии насыщения а ’и А’, давлением насыщенного пара pn, температурой Tn и скрытой теплотой испарения можно получить следующим образом: если жидкость превращается в пар, то давление насыщенного пара не зависит от объема системы, поэтому формула Жидкость в паре происходит при постоянной температуре(7,, = sop8 |)、 Но с момента равновесного преобразования Здесь У представляет собой изменение объема системы при переходе от жидкости к пару.
Кроме этих напряжений трения, нормальные напряжения существуют во всех плоскостях. Людмила Фирмаль
Подобный этому 4rp 15 АГК-Ай. Если жидкость в массе um испаряется, то изменение объема системы равно следующему: (Ив =(о *-о ’)1м、 И (9.28) приращение энтропии в квазистатическом процессе испарения жидкости по массе um аз = — Т» Если присвоить эти значения выражению (9.31), то получится: (9.32) Вот производная давления от температуры на кривой фазового равновесия p» = /(T»). Уравнение(9.32) называется уравнением Клапейрона-Клаузиуса и используется при исследовании изменения сопряженного сопряжения вещества из жидкого состояния в парообразное. Аналогичное уравнение можно применить и к процессу перехода вещества. От твердого к жидкому или газообразному.
Параметры влажного насыщенного пара при заданной сухой величине можно определить из следующих соотношений: Удельный объем увлажненного насыщенного пара Б =(1-Х) О ’+ хо -. (9.33) Объем воды (1-х) мал по сравнению с объемом пара, и поэтому при низком давлении в = НВ. (9.34)) Ввиду того что энтальпия влажного насыщенного пара должна преобразовывать тепло xg kJ1kg в пар X kg жидкости、 Энтропия влажного насыщенного пара Свойства перегретого пара существенно отличаются от свойств насыщенного пара, которые приближаются к свойствам газов.
Перегретый пар характеризуется тем, что при одном и том же давлении температура выше температуры испарения т«, а при одном и том же давлении удельный объем больше объема сухого насыщенного пара. Р =количество тепла, необходимое для передачи 1 кг сухого насыщенного пара через сопло! В перегретом состоянии температуры I, называемом перегретым теплом di, уравнение Если СЛТ-это средняя массовая теплоемкость перегретого пара при постоянном давлении、 7o =Слт (7 ′ — т -). (9.38) Значение с Получается для перегретого пара по формуле: Энтальпия перегретого пара «Н = [„+’1Н =“ + ’+ с „т(т-т“) (9.39) Она называется суммарной теплотой перегретого пара.
Согласно первому закону термодинамики 7 » = и «- и»+/, _(9.40) Где/ = p (op-o») — работа расширения в изобарном процессе перегрева пара. А»и» — изменение внутренней энергии в процессе перегрева. Изменение энтропии в равновесном изобарном процессе перегрева 3″ = е «+ с» | P_G_ = 4,18651 н — ^ в-4-С.. 1n.
Смотрите также:
| Водяной пар. Парообразование при постоянном давлении | Т-S-диаграмма водяного пара |
| Изменение агрегатного состояния | I—S-диаграмма водяного пара |
