Оглавление:




Спектры люминесценции
- Спектр излучения Согласно определению С. И. Вавилова, люминесценция является избыточной люминесценцией по температуре и имеет длительность 10_1 ° с или более, превышающую период колебаний света. Он отличается от излучения нагретого объекта тем, что он не сбалансирован.
- Люминесценцию часто называют холодным светом, потому что он фактически не использует тепловую энергию излучающей системы. Это определение Инвалидность от всех других типов неравновесного свечения и рассеяния света, комбинационного рассеяния, бабил-челенковского излучения и т. Д.
Люминесценция возникает в результате электронных переходов, когда частица возвращается из возбужденного состояния в нормальное состояние. Людмила Фирмаль
Поэтому молекулы превращают поглощенную энергию в собственное излучение. Это также различает процессы излучения света и несоответствующего излучения-рассеяния света и отражения. Люминесцентный материал будет находиться в любом агрегированном состоянии.
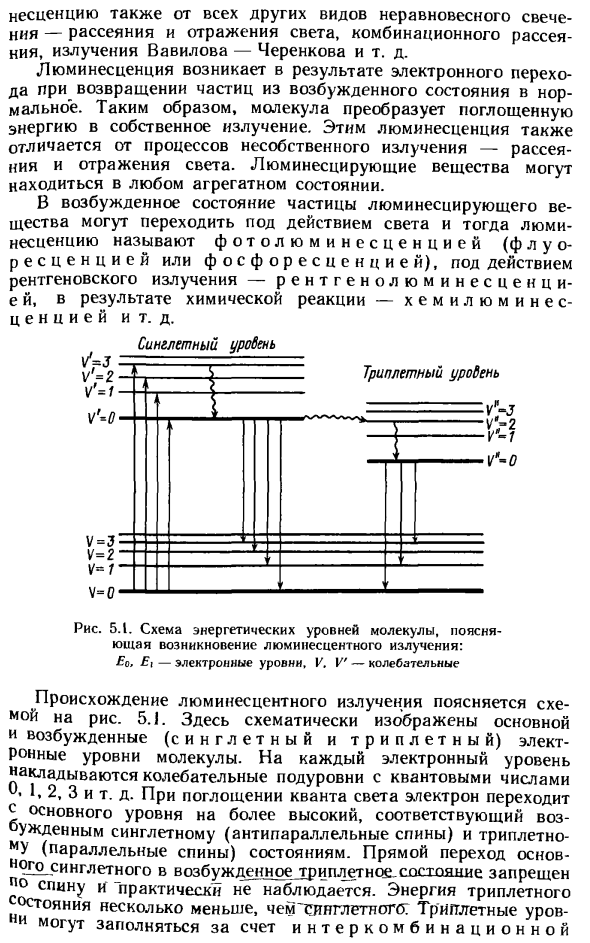
Люминесцентные частицы могут возбуждаться под воздействием света, а затем, под действием рентгеновской эмиссии-рентгеновской эмиссии-хемилюминесценции в результате химической реакции, происходит эмиссия фотолюминесценции ( Г) называется флуоресценцией или фосфоресценцией. Синглетный urobei VFJ Тройной уробей VrJ V’-2 V-1 V’-о V = J V = 2Vе1 4 = 0 Рисунок 5.1.
Диаграмма уровней молекулярной энергии, объясняющая возникновение свечения: Е0, £ г-электронный уровень, В. V ‘-вибрация Происхождение люминесцентного излучения поясняется схемой на рисунке. 5.1. Здесь схематически показаны молекулярные основания и уровни возбуждения (синглетный и триплетный) электронов.
Когда вибрационные подуровни, такие как квантовые числа O »K 2 и 3, накладываются на каждый электронный уровень и квант света поглощается, электроны возбуждаются с основного уровня до возбуждения синглетным (антипараллельный спин) и триплетного MU (параллельный спин). ) Перейти на более высокий уровень, соответствующий состоянию.
Прямой переход от основного синглета к возбужденному триплету. Государство запрещено. С обратной стороны: «На самом деле это не наблюдается. Энергия триплетного состояния немного меньше, чем ~ iagletnogb. V ‘= 2 V = 1 Конверсия (волнистая стрелка V6 = 0, V ‘= 2). При комнатной температуре молекула обычно находится в основном состоянии, и почти все электронные переходы при поглощении света происходят от нижнего (основного) колебательного подуровня возбужденного синглетного состояния к различным колебательным подуровням.
Рисунок 5.1 Эти переходы обозначены стрелками: V = 0 V ‘= 0; = V = 0 Y «= 2 такие как Возбужденные молекулы за счет так называемой колебательной релаксации при столкновениях с окружающими молекулами очень быстро теряют избыточную энергию колебаний по сравнению со временем перехода электрона и переходят на основной уровень колебаний возбужденного электронного (синглетного) состояния. Рисунок 5.1 Этот процесс обозначен волнистой стрелкой. V ‘= 3 V’ = 0; V ‘= 2 V’ = 0; V ‘= 1 V = 0 и т. Д.
Квант света испускается, когда происходит переход от основного колебательного подуровня возбужденного синглетного состояния к колебательному подуровню основного электронного (синглетного) состояния. Этот процесс называется флуоресценцией. Рисунок 5. 1 Переход V0 = 0 Соответствует V = 0. V’o = 0 V = 1; V’0 = 0 + V = 2 и т. Д. Время затухания флуоресценции составляет от 10-9 до 10-7 секунд.
Возбуждение возбужденных молекул также может быть вызвано безызлучательными переходами внутренней конверсии. В триплетном и возбужденном синглетных состояниях происходит колебательная релаксация, и электроны переходят на более низкие колебательные уровни в триплетном состоянии (волнистая стрелка V «= 2 Y» = 0; Y «-1 V» = 0 ). Запрещенные спином радиоактивные переходы триплет-печатка (такие как V «= 0 V = 0; V» = 0 V = 1) называются фосфоресценцией.
- Время жизни триплетного состояния велико (10 3 … 102 секунд). Переход из триплетного состояния в основное синглетное состояние также происходит, когда возбужденная частица сталкивается с окружающими молекулами из-за безызлучательного процесса внутреннего превращения, который имеет очень высокую вероятность при комнатной температуре.
По этой причине образцы обычно замораживают при температуре жидкого азота (77 К), чтобы наблюдать фосфоресценцию и использовать ее в аналитических целях. Спектр фосфоресценции сдвигается в сторону более длинных волн на величину, пропорциональную энергии колебательной релаксации триплетного состояния.
Это минимизирует возможность безызлучательных переходов. Людмила Фирмаль
В зависимости от частоты облучаемого излучения частицы преобразуются в энергетически различные возбужденные состояния, поэтому ожидается связь между спектром флуоресценции и спектром возбуждения источника. На практике, однако, эта зависимость обычно не наблюдается.
Независимость спектра флуоресценции от длины волны падающего света в основном обусловлена колебательной релаксацией в результате того, что возбужденные молекулы тратят энергию колебаний за гораздо более короткое время, чем время жизни возбужденного состояния, и основное состояние возбужденного электронного состояния. Это связано с тем, что у вас есть время, чтобы достичь уровня вибрации.
Переход в невозбужденное состояние такой системы характеризуется тем же излучением фотонов, то есть тем же наблюдаемым спектром флуоресценции. В то же время в некоторых случаях это открывает возможность люминесцентного анализа и позволяет избирательно возбуждать определенные соединения. На рисунке 5.1 показано, что можно ожидать определенного сходства между спектром поглощения вещества и его спектром флуоресценции.
Это потому, что оба определяются по существу одинаковыми электронными переходами. Конечно, аналогичные и установленные законом Стокса-Рома, общий спектр излучения и его максимум всегда смещены в сторону более длинных волн по сравнению со спектром поглощения и его максимумом. , Эта закономерность может быть легко объяснена схемой, показанной на рисунке. 5.1.
Энергия флуоресцентного кванта должна быть меньше энергии поглощенного кванта из-за количества потерь энергии при колебательной релаксации в возбужденном электронном состоянии и переходе на второстепенный колебательный подуровень основного электронного состояния. Спектр излучения большинства материалов характеризуется широкой полосой излучения (100-200 нм).
Однако, если материал исследуется в условиях сильного охлаждения (жидкий азот 77 К или водород 20 К), спектр будет квазилинейным с допустимой колебательной структурой (эффект Сполльского). Поскольку многие соединения способствуют внутримолекулярным взаимодействиям и другим типам взаимодействий, этот эффект проявляется не во всех веществах.
Смотрите также:
Решение задач по аналитической химии
| Общая характеристика атомно-абсорбционного спектрального метода | Энергетический и квантовый выходы люминесценции |
| Задачи по атомно-абсорбционной спектрографии | Интенсивность люминесценции |
