Оглавление:


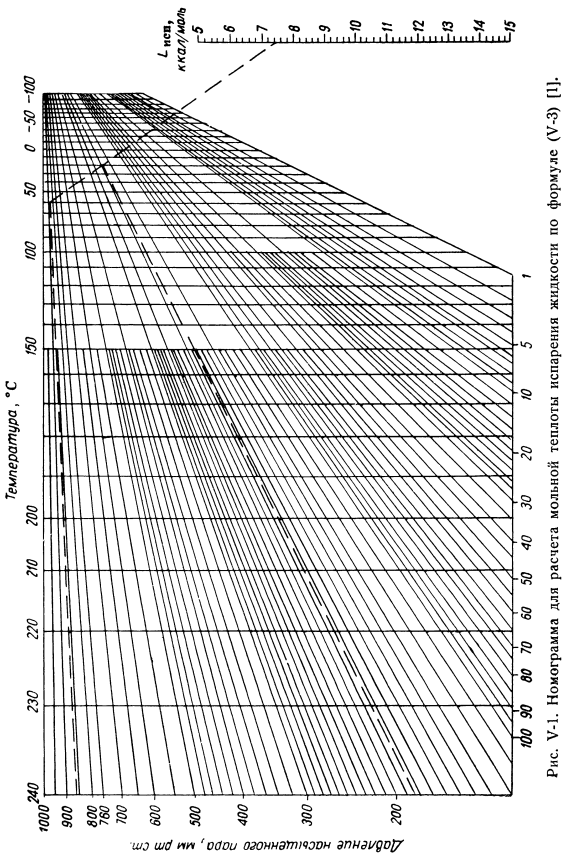




Теплота испарения жидкости
Теплота испарения жидкости. При определенной постоянной температуре давление насыщенного пара над отдельной жидкостью является прозрачным и постоянным. Жидкая и газовая фазы(пар) находятся в состоянии равновесия, при приложении тепла (без изменения температуры и давления) определенное количество вещества переходит из жидкой фазы в газовую. 1 тепло, поглощенное в ходе изотермических и изобарных процессов, при которых жидкость в моле переходит в состояние насыщенного пара, называется теплотой испарения моля (испарительной энтальпией). 1 * зависимость между молярной теплотой испарения psa и зависимостью давления насыщенного пара (rp) от температуры, температуры (T) и изменения объема системы выведена из уравнения Клапейрона-Клаузиуса.
Если мы не введем показанное упрощение, вычисление значений по уравнению Клапейрона-Клаузиуса дает точные результаты. Людмила Фирмаль
- Молярный объем жидкости; Y-механический эквивалент тепла. Применяя общую форму уравнения состояния реального газа к насыщенной паре и преобразуя уравнение (V-!), Получена зависимость. (У-2) Здесь Dg = gy-gf-разность коэффициентов сжатия газа、 Жидкость / ?Это газовая постоянная? Для области низкого давления приблизительно применимо уравнение состояния идеального газа. Уравнение (В -!От), это выглядит так: провайдер〜 −4, Чарли. При преобразовании и консолидации последней зависимости она выглядит следующим образом: (Ю-З) НПС4,57 ЛТ-Г1? ( ^ ) 7 * 2-L Используя формулу (U-3), можно рассчитать приблизительное значение молей теплоты испарения в следующих случаях: значения pg и p1 давления жидкого насыщенного пара известны при температуре T2nT1 (°к).
Для быстрого определения / приближения по формуле (U-3) можно использовать номограмму, показанную на рисунке. У-1. Пример V -!。 Давление насыщенного пара в ацетоне при 20°С равно 184,8.Или » Меркурий.«Статья 60°С-860.8 мм рт. Искусство. Рассчитайте теплоту испарения. Решение. Рисунок\ M рисует линию, соответствующую давлению 184,8 макс. Искусство. Пересечение с изотермами+205С и линией, соответствующей давлению 860,8 мм рт. ст., пересечение с изотермами+ 60ЕС. Полученные точки изотермы соединяют прямой линией, продолжая ее по шкале 7CSa и получая целевое значение 7psp = 7,5 ккал / моль. Теплота испарения, рассчитанная по уравнению (U-W), составляет 7490 кал / моль. Экспериментально установлено, что 7 ОСП = 7220 кал / моль. „ Однако сумма, необходимая для расчета (особенно yrp / yT), обычно неизвестна, поэтому использовать эту формулу сложно. Используя дифференциальный метод Дугласа-авекана, получаем уравнение[2]. провайдер Ягу. Д. * Армированный пластик. (У-4) 397, 7. 1512L, 216 А. /
- Формула (U-4) может быть использована, например, если известно 7 значений давления насыщенного пара при 7 температурах и каждое последующее значение больше на/ г, чем предыдущее. Величина k в случае непрерывного повышения температуры изменяется от −3 до+3 (через 0).Формула (Y-4) определяет значение D, cn при температуре, соответствующей k = 0.Величина Dg указывает на коэффициент сжатия пара(область низкого давления Ar “ 1). Пример U-2. Рассчитайте теплоту испарения воды при / −30°C температурной зависимости давления пара: /, °С15 20 25 30 35 40 45 РП, мм рт. ст. 12.79 17.54 23.76 31.82 42.18 55.32 71.83 Решение. 1.It следует формуле (Y * 3). Данные. / , = 25°C; 7 * 1 = 298,2 E K; p,= 23,76 мм рт. ст. ИСП.4.57•298.2•308.2• 308.2-298.2 42.18. 23.76. = 10 430 кал / моль / 2 = 35°С; Г2 = 308.2°к; Р2 = 42.18 мм рт. Искусство. 2.По формуле (U-4). От 15°С-при 3, 20°С2.
При температуре 25°C, например, A = −1; Dg » 1; 7 = 303,25 K; L = 5. (-3)-12.79 4-(-2)-17.54-±<-1)-23.76 + 031.82 + 1 −42.18 + + 2-55.32 + 3-71.88 = 271.27 2 к * п=(-3)»-12.79 +(-2)3-17.54 +(—Я)3•23.76 + О3 * 31.82 + + I3•42.18 + 23•55.32 + З3.•71.88 = 1916.22、1.985-303.22 / 397-271.27 7-1916.22 \ 1Р…. = 31.82 (PHPPZ 2T6T5—)= 10445 КАЛ / М°Л Найдено экспериментально/, ICO » 10452 кал / моль. В приведенном выше примере предполагается, что уравнение состояния для идеального газа может быть применено к преобразованию с участием насыщенного пара (Λ= 1).Часто это приводит к большой ошибке. / АРМИРОВАННЫЙ ПЛАСТИК 1 тонна Хаггенмахер [3]показал значение Dg как функцию заданного параметра.
При температурах, далеких от критических, молярный объем жидкости пренебрежимо мал, поскольку он очень мал по сравнению с молярным объемом пара. Людмила Фирмаль
- Пр * 3 пиар. ±Р = Л / 1 ^(Г-5) Куда? pn = pn (где pk-пониженное давление насыщенного пара, а 7 ^ = G / Gkr-пониженная температура. ’ИСП. 1.^ прпр г 1П РТС На G3. пиар. (Т) (У-6) Из уравнений (U-2)и (U-5): Если известна температурная зависимость давления насыщенного пара, то можно рассчитать значение отношения c (\p pn / s1 (\/T) очень accurately. In в этом случае погрешность расчета по формуле (Y-6) обычно не превышает±1. Расчет величины (1ппрп/ / / / / / ц\\) можно исключить, если известно уравнение для температурной зависимости давления насыщенного пара. Например, если такая зависимость дана в виде эмпирической формулы Антуана ’КПН = -р ^ г-(г-7) И затем… Что это такое? (с ’ + Ту Где c ’ константа, которая была изменена подстановкой/
