Оглавление:



Возрастание энтропии изолированной системы при неравновесных процессах
- Принцип возрастания энтропии часто формулируется следующим образом энтропия изолированной системы всегда возрастает при наличии неравновесности процесса. В данном случае под изолированной системой понимается совокупность взаимодействующих объектов. Фактически, учитывая взаимодействие термодинамической системы с окружающей средой, разделенные системы, очевидно, будут представлять собой их комбинацию, и изменение их энтропии будет составлять 45c. C 45 34-45 уравнение 7.
Изменение энтропии термодинамической системы согласно 45-0 изменение энтропии термодинамической системы. Энтропия окружающей среды отсутствует. 45 p l или позже Если, 13, знак противоположен, а абсолютное значение равно 45 0 45 r, Если 45 положительно, то 45×45 ri, 45е 3 отрицательно, следовательно, 45c 0, то есть вследствие неравновесного процесса энтропия изолированной системы возрастает. Приведем пример, показывающий разницу в поведении энтропии изолированной системы при неравновесном процессе и равновесном процессе.
В области теплообмена интересуются главным образом тепловым потоком приходящимся на единицу площади поверхности тела. Людмила Фирмаль
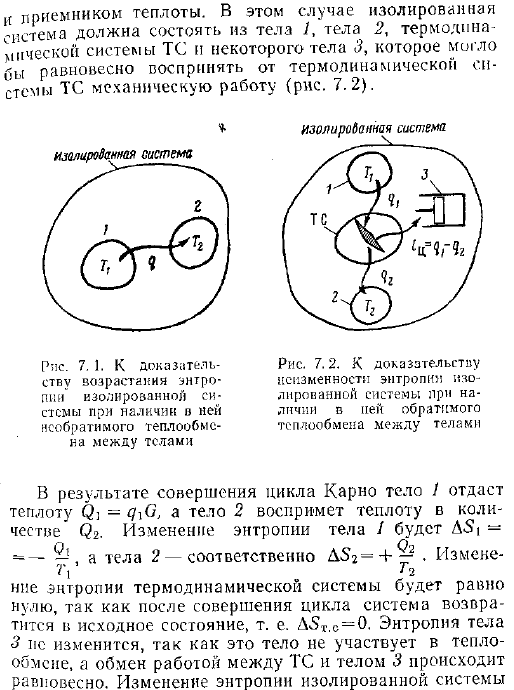
Предположим, что 2 объекта с различными температурами t a являются изолированными системами и находятся в тепловом контакте друг с другом рис. 7. 1. В этом случае, очевидно, происходит неравновесный теплообмен. Изменение энтропии всей системы Д и. С тА 14 2—- Л. Где 2 — количество тепла, передаваемого от тела 1 к телу 2. 7 2 или позже, d5i. C 0, то есть энтропия изолированной системы, в которой присутствует необратимый теплообмен, возрастает.
- Если теплообмен между и 2 объектами осуществляется в равновесии, то требуется промежуточное звено-термодинамическая система, способная завершить цикл Карно. Источник тепло sink. In в этом случае изолированная система делится на d-Кузов 2, термодинамическую систему транспортного средства и некоторый Кузов 3. Они находятся в равновесии и принимают механическую работу от термодинамической системы транспортного средства рис. 7. 2. Рисунок 7. 1. О доказательстве увеличения энтропии системы разделения при наличии необратимого теплообмена между объектами. Рисунок 7. 2.
Доказательство инвариантности энтропии изолированной системы при наличии обратимого теплообмена между объектами шарпея В результате цикла Карно тело 1 отдаст тепло И тело 2 забирает тепло в количестве 2. Изменение энтропии в теле 1 равно d 1-и тело 2 равно d32 h — g соответственно. Энтропия термодинамической системы равна нулю. После завершения цикла система возвращается в исходное состояние, т. е. D5tc 0. Энтропия тела 3 не изменяется. Тело 3 находится в равновесии.
Уравнения (16-23а) и (16-236) описывают соответственно поток тепла, обусловленный теплопроводностью, и диффузионный поток массы. Людмила Фирмаль
Изменение энтропии изолированной системы — — Есть, и поэтому при абсолютной величине отношения равны, то есть i—- Л Г2 1 1 Таким образом, энтропия изолированной системы в Наличие только равновесных процессов в нем не изменяется Д5Я. С 0. Контрольный вопрос 1. Каковы основные особенности неравновесного процесса 2. Могу ли я изменить энтропию в процессе без теплопередачи теплоизоляции 3. Что называется вечным двигателем второго рода 4. Как я могу передать тепло от высокотемпературного объекта к низкотемпературному объекту, используя только обратимый процесс 5.
Смотрите также:
| Второй закон термодинамики | Основные понятия о движении газов |
| Возрастание энтропии термодинамической системы при неравновесных процессах | Уравнение расхода |
