Оглавление:


Ϭ-, π- и ẟ-Связи
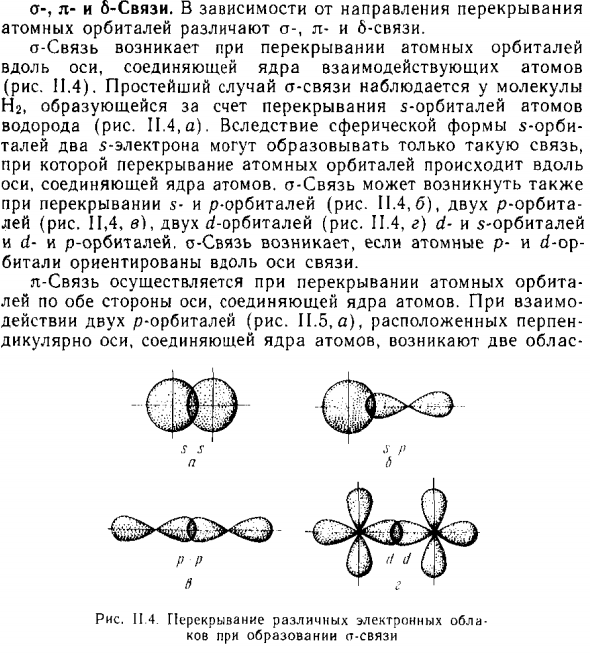
- Ϭ-, π- и ẟ-Связи. Зависит от направления перекрытия Атомные орбитали различают связи a, l и 6. Связь возникает, когда атомные орбитали перекрываются Вдоль оси, соединяющей ядра взаимодействующих атомов (Рисунок 11.4). Простейший случай а-связи наблюдается с молекулами Ng, образованный в результате перекрытия пяти атомных орбиталей Водород (рис. 11.4, а).
- Для сферы 5 орбит Два 5 электрона могут только сформировать такую связь. Атомное орбитальное перекрытие происходит вдоль Ось, соединяющая ядра. А-связь также может возникнуть Когда p орбиты перекрываются с 5 орбитами (рисунки 11.4 и 6), 2 p орбитали лей (рисунки I, 4, с), два Орбита (рисунок I, 4, d) и «-орбит» А р-орбитали, атомные р и ¿
Жизненно важные органы ориентированы вдоль оси связи. i-связи выполняются путем перекрывания атомных орбиталей. Людмила Фирмаль
Лучи по обе стороны от оси, соединяющей атомные ядра. между Работа двух p-орбит (рис. 11.5, а), размещенных на груше Встречаются две области, особенно относительно оси, соединяющей атомные ядра. R P но Ты дублирован. Следовательно, связь L равна 2 Перекрывающиеся области с обеих сторон оси, Подключите ядра. л-связь р-орбита и ¿ Орбита (рис. 11.5.6) или две The Beatles {рис. 11.5.6).
B связь является двумя ¿ Они размещены в параллельной плоскости (рисунок 11.6). так Поэтому 5 е могут участвовать только в образовании образование связи, р-электрон-связь и связь l; Формирование ny-a связи, l связи и b связи. далее Различные способы взаимодействия электронов. связь l и связь b накладываются на связь d, и в результате Двойные и тройные связи образуются.
- Например, между атомами Углерод молекулы этилена, одна а и одна связь l образуются. Следовательно, связь между атомами углерода является двойной Двойные связи также возникают во время образования Ноа H 2C = C H 2. Молекула COz (0 = C = 0). Немного кислоты и т. Д. Между атомами углерода молекулы ацетилена связь и две связи, каждая связь между атомами Углерод тройной. H C = CH.
Тройная связь Происходит при образовании молекулы азота L = L. Количество ссылок То, что образуется между атомами, называется г (От ры до приблизительно м) Увеличение коммуникаций и коммуникационной множественности (заказ) Длина связи и ее энергия изменяются. Рисунок 11.7Нелинейный характер.
Связь между энергией и множественностью связей. Людмила Фирмаль
Энергия двойной связи не увеличивается Удвоенная и тройная энергия связи не увеличивается на 3 Время по сравнению с энергией одинарной связи. Это Разница в энергии между связью и связью. Так, например, для подключения Углерод-углерод энергия связи меньше, чем энергия связи. Для азот-азотной связи обратное соотношение.
Смотрите также:
| Валентность | Гибридизация атомных орбиталей |
| Донорно-акцепторный механизм образования ковалентной связи | Пространственная конфигурация молекул |
Если вам потребуется помощь по химии вы всегда можете написать мне в whatsapp.
