| 🎓 Заказ №: 22221 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
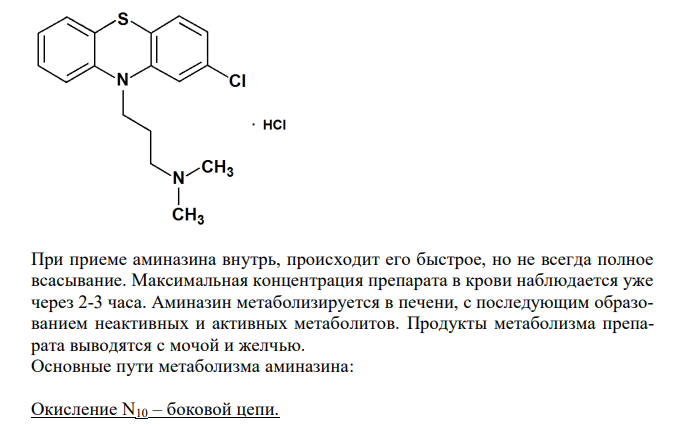
Отразите основные пути метаболизма аминазина. Объясните, чем обусловлена окраска мочи при отравлении аминазином.
Ответ: Аминазин, Хлорпромазина гидрохлорид (Chlorpromazine Hydrochloride) 2-хлор-10-(3´-диметиламинопропил)фенотиазина гидрохлорид 267 При приеме аминазина внутрь, происходит его быстрое, но не всегда полное всасывание. Максимальная концентрация препарата в крови наблюдается уже через 2-3 часа. Аминазин метаболизируется в печени, с последующим образованием неактивных и активных метаболитов. Продукты метаболизма препарата выводятся с мочой и желчью. Основные пути метаболизма аминазина: Окисление N10 – боковой цепи. N-оксид аминазина N-деметилирование

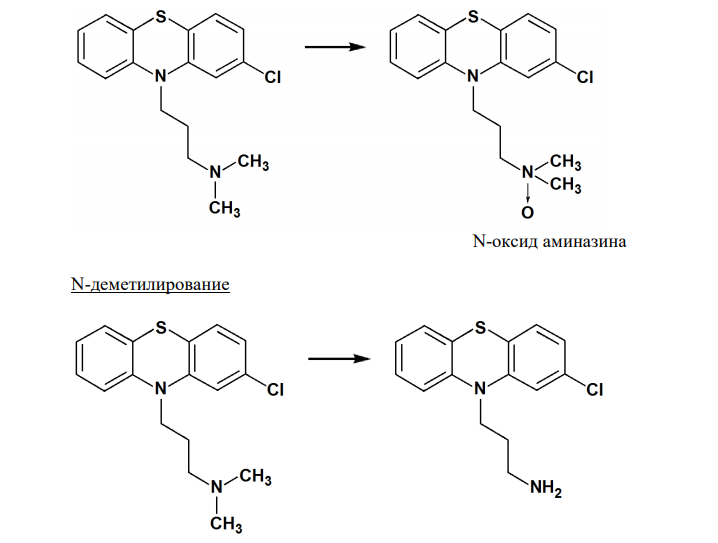
| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Вычислить тепловой эффект реакции при стандартных условиях. С2H5OH C2H4 H2O
- Рассчитайте pH и pOH растворов c заданной молярной концентрацией (см. свой вариант в табл. 2).
- В реакции между раскаленным железом и паром при достижении равновесия парциальные давления водорода и пара равны 3,2 и 2,4 кПа
- Для сплава (см. свой вариант в табл., задание 1) определите возможность коррозии при pH = 4 и 8, запишите коррозионные гальванические элементы и уравнения электродных реакций.
- Определите электронное семейство элементов, указанных в разделе 3.2, распределите валентные электроны по квантовым ячейкам в невозбужденном состоянии атома.
- Осуществите превращения, указанные в цепочке.
- Рассчитайте f H298 и f S298 следующей реакции: 2 2( ) 2 ( ) 1 2Ag(к) O г Ag O к
- Составьте электродные уравнения процессов, происходящих на растворимых электродах (см. свой вариант в табл., задание 2).
- Составьте электродные уравнения процессов, происходящих на инертных электродах, при электролизе водного раствора соли и при заданных условиях (сила тока и время) (см. свой вариант в табл., задание 1).
- Для реакции Ag2O(к) = 2Ag(к) + 0,5O2(г), Hх . р. 31,15 кДж.
