Оглавление:







Белки
- Белки. Повторите из учебника» Общая биология » § 30. Белка-это он. Азотсодержащее высокомолекулярное органическое вещество со сложным составом и структурой молекул. Белок является основным компонентом пищи наряду с углеводами и жирами. Все жизненные процессы связаны с белками. Фридрих Энгельс в своей книге»противоядие»пишет, что»жизнь-это способ существования белкового тела.»
- Белки являются частью клеток и тканей всех живых организмов. Состав и структура белков. В состав белков входят углерод, водород, кислород и nitrogen. In кроме того, большинство белков содержат серу, а в некоторых случаях фосфор, железо и другие элементы. So например, относительная молекулярная масса белков, входящих в состав куриных яиц, составляет 36 000, а 1 из мышечных белков достигает 150 000.
Молекулярная масса белка очень высока large. Людмила Фирмаль
Некоторые из других белков имеют относительную молекулярную массу более 300 000. В результате гидролиза белков чаще всего получают 20 аминокислот. Если молекула белка содержит только 20 молекул каждой из этих 1 аминокислоты, они являются. При подключении друг к другу, вы получите различные комбинации 2.4•1018 и выше. Поэтому понятно, насколько разнообразна и сложна структура белковых молекул.
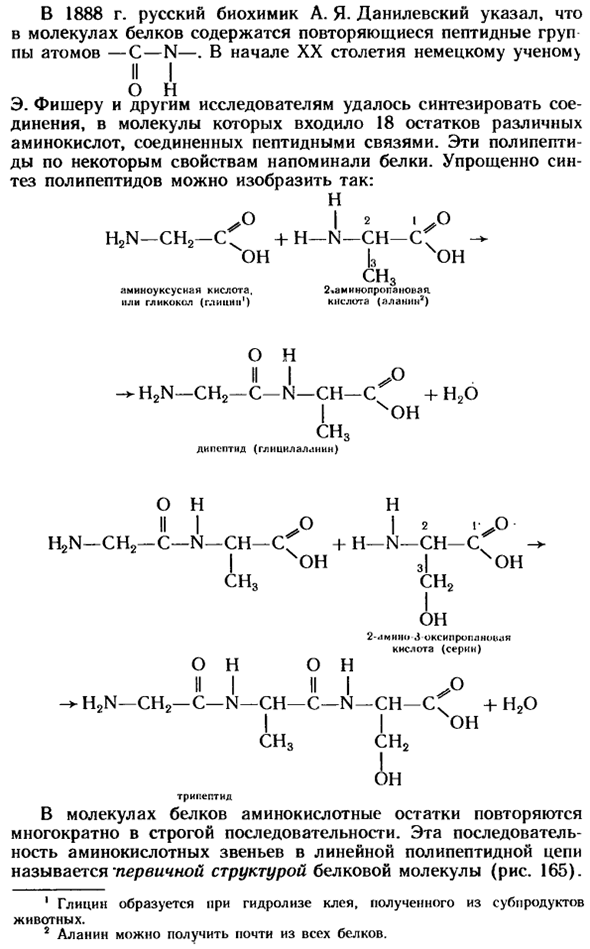
В 1888 году русский биохимик А. Я. Данилевский показал, что повторяющиеся пептидные группы-С-N-атомов содержатся в белковых молекулах. В начале 20-го века немецкие ученые) II I о н Э. Фишеру и другим исследователям удалось синтезировать соединение, содержащее 18 остатков в молекуле различных аминокислот, соединенных пептидными связями. Эти полипептиды по некоторым свойствам напоминали белки.
Упрощенный синтез полипептидов может быть представлен следующим образом: 166.Первичная структура белка. Пространственное расположение белковых молекул подобно спиралям образовано рядом водородных связей между-CO-и-NH-группами (рис.166).Эта структура белка называется вторичной.
В пространстве спирально скрученная полипептидная цепь образует третичную структуру белка (рис. 167), которая поддерживается взаимодействием различных функциональных групп полипептидных цепей. Например, дисульфидное сшивание (- S_S -) часто образуется между атомами серы, и существует сложноэфирное сшивание между карбоксильной группой и гидроксильной группой, и солевой мостик образуется между карбоксильной группой и аминогруппой.
Вода также является особенностью этой структуры. Рисунок 166.Вторичная структура белого цвета. 167.Третичная структура белка. Бухточка. Семейные связи. Третичная структура белка в значительной степени определяет специфическую биологическую активность молекулы белка. Большое количество белковых макромолекул связываются друг с другом, образуя относительно крупные aggregates.
An примером такого белка является гемоглобин, который представляет собой комплекс из 4 макромолекул (рис.168).Только по этой структуре мы можем видеть, что гемоглобин может присоединять и транспортировать кислород в организме. Подобное полимерное образование белков, в котором белковый полимер является мономером, называется четвертичной структурой. Белки являются лучшей формой развития органических substances.
It сочетает в себе свойства различных видов органических соединений, сочетание которых дает совершенно новое качество, имеющее большое значение в жизненных процессах организма. Физические характеристики. Белки не растворяются и не растворяются в воде. Некоторые из них образуют коллоидный раствор с водой. Химическое свойство. 1.Белок характеризуется реакцией на precipitate.
- In в одних случаях образующийся осадок снова растворяется в избытке воды. В других случаях происходит необратимая коагуляция белков, то есть денатурация, в результате чего молекула подвергается необратимому химическому воздействию changes. So например, этанол осаждает белки различными способами. Если воздействовать на яичные белки разбавленным раствором в течение короткого времени, осадок может раствориться в воде.
Но если воздействовать на белок неразбавленным спиртом, то произойдет дегенерация. Белки, содержащие легкие металлы и соли аммония(такие как NaCl, MgS04,ZnS04,(NH4) 2S04), образуют осадок, который может снова раствориться. Но благодаря действию солей и концентрированной азотной кислоты тяжелых металлов (Fe, Pb, Hg и др.), белок необратимо затвердевает.
Такой же результат можно получить при нагревании белка. Людмила Фирмаль
2.Хромогенная реакция белка: а) небольшое количество раствора белка с добавлением небольшого количества гидроксида натрия и капли раствора сульфата меди (II), появится красновато-фиолетовый цвет. Такая же реакция происходит и в других соединениях, содержащих пептидные группы.
Б)когда белка концентрируют с концентрированной азотной кислотой, белок окрасится в желтый цвет. Эта реакция доказывает, что остатки ароматических аминокислот попадают в белок оленя. в) добавляют свинец (II) к раствору белка, а затем, когда гидроксид натрия нагревают, черный осадок сульфида свинца (II) осаждается из-за сочетания серы и свинца.
3.Гидролиз белков. При нагревании белка щелочью или кислотой происходит гидролиз: О, о, о, о. II I II / II NН 2-СН-С-Н-СН-С-Н-СН-С -… + pH20 к р «р’» (^ ^ ) — ►NН 2-СН-с + NН 2-СН-с ^ + NН 2-ч-ср. + | он мне Чон / функция Р Р «Р’» Превращение белков в body. In у животных и человека гидролиз белков происходит под влиянием ферментов (пепсина, трипсина, элепсина и др.).
В результате образуются аминокислоты, которые всасываются в кровь кишечными ворсинками и используются для образования белков, свойственных данному организму. Синтез белка включает в себя поглощение энергии. Молекулы ATP1 обеспечивают это energy. In организм, одновременно с синтезом белков, полностью разрушается, сначала аминокислотами, затем окисью углерода (IV), аммиаком, мочевиной, водой.
Во время этих процессов выделяется энергия, но в меньшем количестве, чем при порче углеводов и жиров. Преуспел в изучении синтеза белка. Те, кто уже изучил белок впервые, дают некоторые представления об очень сложной структуре его molecule. At на современном этапе развития химической науки до сих пор очень трудно определить структуру белковых молекул.
Первым белком, который смог расшифровать первичную структуру в 1954 году, был инсулин (он регулирует уровень глюкозы в крови).Молекула инсулина состоит из 2 полипептидных цепей.1 из них содержит 21, а другой 1 содержит 30 аминокислотных остатков. В настоящее время синтез insulin. To для получения 1 полипептидной цепи потребовалось 89 реакций, чтобы получить еще 138 реакций.
Синтез белков в лабораториях и на химических заводах-очень сложная задача. Решение будет максимальным 1. повторите из учебника» Общая биология » § 31. 45-47. Несчастье всего человечества открывает небывалые ресурсы для получения различных веществ и материалов для потребительского потребления и технологии.
Решается проблема производства биохимических и синтетических продуктов питания (проводятся обширные исследования в этой области).N. задача ликвидации многих болезней станет реальностью. ** I. какие элементы входят в состав белка? Объясняет структуру белковых молекул. 2.Каковы наиболее характерные группы атомов и типы связей большинства белковых молекул? 3.Где находится белок в природе и в чем его важность?
4.Опишите физические и химические свойства белка. 5.Как можно доказать наличие белка в пище, в шерстяных и шелковых тканях? 6. Сколько различных трипептидов может быть образовано комбинацией из 3 аминокислот (необязательно).Создайте уравнение для соответствующей реакции. 7.Какие вещества образуются при гидролизе белков в организме?
Дается общее описание роли белков в критических процессах у человека и животных. 8.Какова роль ДНК и РНК в биохимических процессах человеческого организма? Какова роль нуклеиновых кислот в регуляции механизмов наследственности? 9.В чем заключается сложность синтеза белка? Как химики решают эту проблему сейчас?
Каковы достижения в этой области? И какие задачи будут решаться в будущем? Лабораторные опыты Растворение и осаждение белка. 1. Влейте в колбу 2-3 мл яичного белка, добавьте 15-20 мл воды и взбейте. В пробирку наливают 2,2-3 мл полученного раствора белка и добавляют 0,5 мл раствора для разбавления этанолом. 3. Влейте 10-15 мл воды в белковую суспензию и встряхните.
Денатурация белка. I. в пробирку наливают 2-3 мл воды и предварительно приготовленный белковый раствор и добавляют 1-2 мл неразбавленного этанола. 2. Налейте 10-15 мл воды в пробирку вместе с гранулами и встряхните. Задача. Почему при действии белков неразбавленным спиртом образуется водонерастворимый осадок? Цветовая реакция на белки. Биуретовая реакция.
В пробирку наливают 2-3 мл раствора белка, добавляют несколько миллилитров раствора гидроксида натрия, затем небольшое количество раствора сульфата меди (II). Реакция ксантопротеина. В пробирку наливают 2-3 мл белкового раствора и добавляют 0,5-1 мл концентрированной азотной кислоты. Задача. I. Как можно доказать наличие белка в пище? 2.В чем суть цветовой реакции белков? Свойства капрона. 1.Используйте тигель для нанесения образца нейлонового волокна на пламя горелки.
2.Принесите влажную красную лакмусовую бумажку к перегару. 3.Положите небольшое нейлоновое волокно в фарфоровую чашку и нагрейте его. 4.Попробуйте вытащить нить из расплавленного волокна с помощью стеклянного стержня. 5. Положите небольшое волокно нейлона в 4 tubes. In в первой пробирке азотная кислота (о = «1,4 г / см3»), во 2-й серная кислота (о = 1,84 г / см3), в 3-й-раствор гидроксида натрия, в 4-й-ацетон.
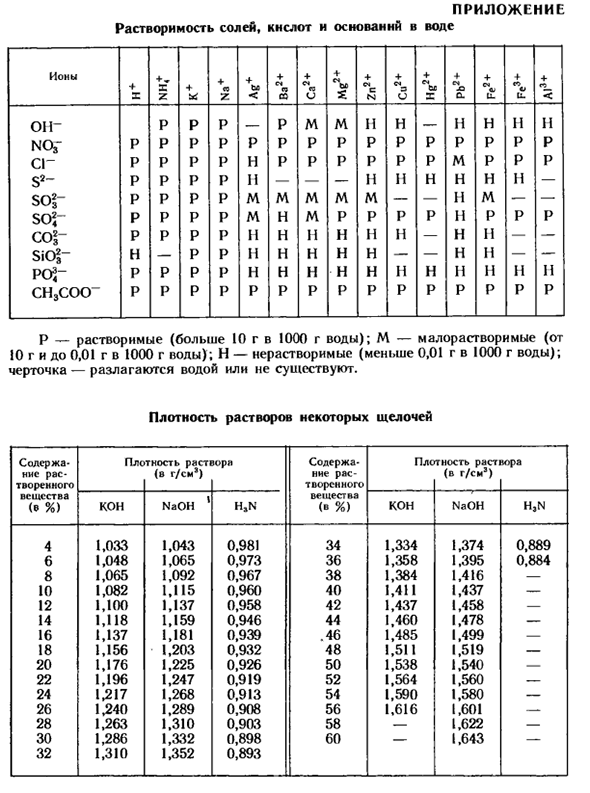
Через 10 минут содержимое пробирки смешать со стеклянной палочкой. Задача. Как вещество первой, второй, третьей и четвертой пробирок влияет на нейлон? Используйте таблицу (приложение, стр. 282-283), чтобы узнать характеристики нитрона и лавсана. Практика 4 Решение экспериментальных задач. 1.Получают этилен и ацетилен, проводят эксперименты на них и подтверждают их характерные свойства. Создайте уравнение для соответствующей реакции.
2.Вещество помещают в 2 пробирки. этанол. б)глицерин. Проведите эксперименты, чтобы проверить их характеристики. Напишите уравнение соответствующей реакции. 3.Вещество помещают в 2 пробирки. бензол. б) уксусная кислота. Проведите эксперименты, чтобы проверить их характеристики. Создайте уравнение для соответствующей реакции. Опишите уравнения реакции, связанные с уксусной кислотой в виде молекул, ионов и укороченных ионов.
4.Дают фенольный раствор в одной пробирке и метанальный раствор в другой пробирке. Проводят эксперименты по проверке их характерных химических свойств. Напишите уравнение соответствующей реакции. 5.2 пробирки с веществом: а) глюкоза. б) сахароза. Определите эти вещества с помощью характерных химических реакций и составьте соответствующие уравнения.
6.Следующие вещества: раствор этанола, пропанола, муравьиной кислоты, уксусной кислоты, серной кислоты. Получите 4 различных эфира и создайте соответствующие уравнения. 5. решение экспериментальных и вычислительных задач в области неорганической и органической химии. 1. Дайте 0,05 литра воды и соответствующее количество нитрата натрия. 5 месяцев для приготовления раствора, содержащего 0,12. d. или 12% этого вещества.
2.Дайте достаточное количество соляной кислоты. Рассчитайте количество цинка, необходимое для получения 200 мл водорода(N. a. it это не так. Возьмите этот газ и соберите его. 3. in vitro сульфат натрия Великого Короля 0,5 г. рассчитайте количество хлорида бария, необходимое для полного осаждения сульфат-ионов. Мы проводим эту реакцию на практике и определяем массу полученного осадка.
К реакции (III) добавляли 4.2.5 г гидроксида железа. Рассчитайте необходимое для этого количество хлорида железа (III), если 5 месяцев содержит 0,1. d. или 10% из impurities. Do это реакция на практике. 5.В пробирку вводят следующие вещества. а)этанол, глицерин, метаналь и решений. б) растворы глюкозы, уксусной кислоты и фенола.
Определите каждое вещество эмпирически и напишите уравнение соответствующей реакции. Ученичество 6 и 7 Опознавание пластмассы и волокна. Перед началом фактической работы ознакомьтесь со свойствами пластика и волокна(приложение, стр. 278-283).Затем получите задание от учителя. Пластическое восприятие следует начинать с внешнего осмотра, а затем исследовать взаимосвязь между нагревом и горением.
Затем его подвергают воздействию растворителя. Восприятие волокна начинается с burning. At одновременно контролируется скорость горения, исследуется запах продуктов разложения, характеристики остатков, образующихся после горения. Далее, проверьте действие на волокна кислот, щелочей и растворителей. Было выдано 1,4 пакета пластиковых образцов.
а) поливинилхлорид, аминопласт, целлулоид, фенопласт. б)полиэтилен, полистирол, полиметилметакрилат и капрон. Проверьте, какой пластик находится в каждой сумке. Было выдано 2,4 мешка с образцами ткани. B) хлопчатобумажная ткань, ацетатное волокно, хлорин, нейлон. Определите, какие вещества находятся в каждом мешке.
Смотрите также:
| Амины | Понятие о материи и веществе |
| Аминокислоты | Определение химии |
Если вам потребуется помощь по химии вы всегда можете написать мне в whatsapp.
