Оглавление:

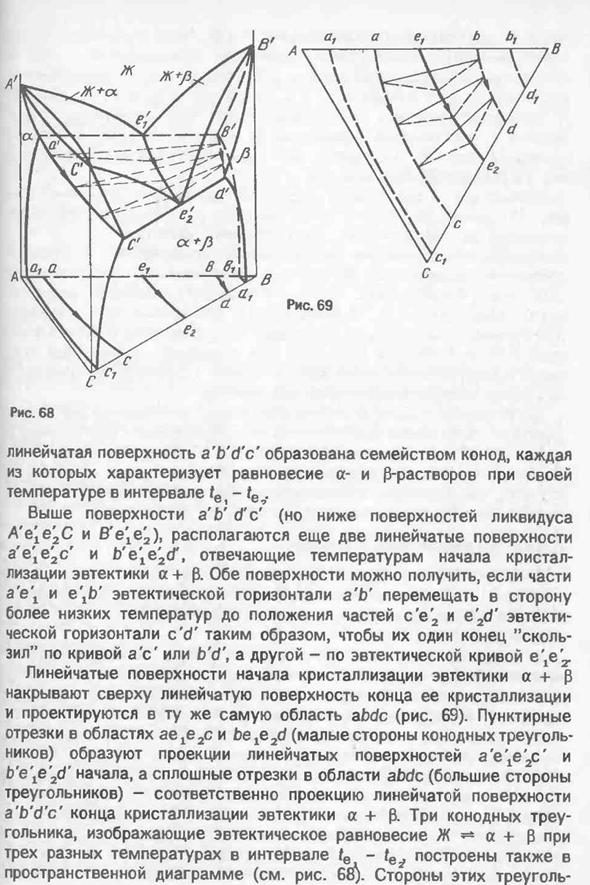












Диаграмма состояния системы с моновариантным эвтектическим равновесием
- Диаграмма состояния системы, имеющей моновариантное эвтектическое равновесие W-a+P (рис. 68) образуется эвтектическим типом двух двойных систем A-B и B-C и систем a-C с непрерывными рядами жидких и твердых a-растворов. Граничное решение, основанное на компоненте B, обозначается как p. Система ликвидуса образована двумя поверхностями AE\e ’ 2C ’и B’E’ 2, соответственно соответствующими температуре начала кристаллизации границы a-и p-растворов. Названные поверхности пересекаются вдоль эвтектической кривой e\e ’ 2.
Концентрация поверхности жидкой фазы на плоскости треугольника и эвтектической кривой проецируется на область и граничную кривую e^aeche2c и Vege2 первичной кристаллизации а-и Р-растворов. Тальвег-буквально «русло реки», т. е. Линия, соединяющая нижние точки эвтербедской » долины «между двумя» горными склонами » и поверхностным типом ликвидуса). Твердая поверхность состоит из трех различных поверхностей. Две поверхности a’A ’и VGSG(разработанные с AACC и BBD) соответствуют температуре в конце кристаллизации растворов A и P, а третья поверхность a’bdc’-это температура в конце кристаллизации эвтектики a + b. горизонтальной C’d ’
на пространственной диаграмме эвтектическая горизонтальная a’b’(Система A-B) перемещается в положение эвтектической Людмила Фирмаль
(система B-C) в сторону более низкой температуры, так что эта поверхность может быть получена., 122linear поверхности б б ’с с’образованной семье conords, что характеризует равновесие а-и 0-решение в GW1-т е м температура на поверхности а б б ’с’(и если обе поверхности могут быть получены, части В Е Х и Е Е и Е Е Х Х Х Х Х’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’ Х ’Х, так что эвтектической горизонтали с б’ 69). Пунктирные сегменты в области aege2c и bethe2d (малые стороны конодныхтреугольников) образуют первую проекцию линейной поверхности a’e\e’2C’ и b’E^e^d’, а сплошные сегменты в области abdc (три коноды, представляющие собой совместное уравновешивание Ω-a+0 треугольника) также состоят из трех различных температур в пространственной диаграмме см. . 68\стороны этих треугольников-
След от разреза в трех горизонтальных плоскостях в пространстве 123º графа этих треугольных вершинных кривых изменяет состав этих фаз во время кристаллизации ковалентного a+p в области ABDC сплавов, где поверхность доминирует в начале и конце кристаллизации эвтектического a+r(см. пункт 2). Кривая a’C ’и b’d’(рис. 68) эвтектика А + Р характеризует не только состав а-и Р-кристаллов, выделяющихся из жидкости при кристаллизации, но и максимальную взаимную растворимость компонентов в твердом состоянии. Кривая а представляет собой максимальную растворимость компонентов в компонентах а и с, кривая б» — наоборот, растворимость компонентов А и С в компонентах в, обе кривые часто выражаются двумя
- растворимостями изотерм1с1 и в1д1 на плоскости треугольника, растворимость компонентов А и С в твердом состоянии в плоскости треугольника. Две поверхности сольвуса проходят через Кривую a’C ’и tc v b’ и в пределах пространственной диаграммы. Переменная растворимость компонента B в компонентах A и C представлена поверхностью a^ ’ c’c’c v a в компоненте A, а компонента B-поверхностью B1b’dr 69 на плоскости концентрационного треугольника). 2. Фазовое превращение сплавов a^C и b^G (рис. 70) как кристаллизованный-и Р-раствор, не претерпевает фазового превращения и имеет две важные точки На кривой охлаждения при охлаждении в твердом состоянии(§ 34).
Сплавы соседних областей a^c C j и b1bddl также заканчивают кристаллизацию в виде A-и p-растворов, но при охлаждении в твердом состоянии в результате вторичной кристаллизации образуются две фазы a+r 70, a). Состав первого кристалла а, который выделяется из жидкого состава точки 1 в этом сплаве, представлен точкой х, расположенной в области ААСС. В интервале кристаллизации жидкость меняет свой состав по кривой 1y^2 в направлении от точки 1 к точке А, а по кривой x X t1 в направлении от точки X к точке 1 соответственно на пространственной диаграмме (см. Рисунок). 68) эти кривые индивидуально установлены на поверхности ликвидуса 124А Райс, семьдесят. С б В е’zs’ и ’ в ’ с ’ Солидус. При определенной промежуточной температуре в интервале кристаллизации состав
Кристалла а и жидкости выражается в терминах XX и YP, а равновесие этих фаз является конодом xx x x x x x x через точку визуализации сплава. Людмила Фирмаль
В этот момент сплав 1 кристаллизуется примерно до половины, так как соотношение сегментов (x x/x x x и 7uh/x x x) и измеряет долю жидких кристаллов X1 и Ah^. Кристаллизация сплава 1 заканчивается, когда Кристалл Ах принимает состав точки 1 (то есть исходный расплав) и жидкий жуз полностью исчезает (см.§ 34). Следует отметить, что жидкая фаза этого сплава исчезает (то есть при более высокой температуре) раньше времени взятия композиции из одной из точек на эвтектической кривой e Xe2. Диапазон температур между твердым телом и поверхностью решателей (поверхности A’A ’ s ’ S ’и ha’ S X на фиг. 68) в сплаве отсутствует фазовое превращение-он охлаждается как ненасыщенный а-раствор.
Как только метафорическая точка сплава 1 оказывается на поверхности сольвуса (эта поверхность проецируется на область а hassx), a-кристаллы насыщаются по отношению к p-кристаллам, а состав температурно-первых вторичных P-кристаллов представлен z-точками, расположенными в области bxddx (на эту область проецируется вторая solvasb’D1). видеть. 68), и первый конод, характеризующий равновесие первичного х — и вторичного (^- Кристалл-каждый сегмент 1z. при понижении температуры до комнатной состав кристаллов Ah-и γ2 не постоянен, а изменяется вдоль пространственных кривых 1×2 и zz2(6=K-f+1=) =3 — 2 + 1 =2!) Из точки x в точку X из точки 1 и z 2 и z7 при комнатной температуре-Кристалл принимает состав из точки x 2 растворимость раствора
изотерма a в^ — Кристалл-соответственно в точке Z 2 Вторая изотерма b t d r результат——— * » x-1 (первичная кристаллизация) и si_ha_______ * _ > Pz_Za (вторичная кристаллизация). Кривая охлаждения этого сплава показана на рисунке. Под микроскопом в структуре сплава можно увидеть два структурных компонента: первичный А-и вторичный Р-Кристалл, выделенные из них(см. рис. 12), определяя соотношение его фракций отрезка 1zx JX£2 и 1×2/x2z2 (см. фиг. 70, а). Кристаллизация сплава 2, находящегося на кривой максимальной растворимости, во многом напоминает кристаллизацию предыдущего сплава 1. Разница заключается в том, что кристалл а сплава 2 насыщается относительно кристалла Р в конце кристаллизации, предполагая состав точки 2. По-видимому, последний след жидкости в этом сплаве имеет состав точки U3, которая расположена на эвтектической кривой e t e2(как
и в сплаве a двойной системы A-B). Таким образом, отделение вторичного р от первичного кристалла а в сплаве 2 начинается, как только он перестает кристаллизоваться. При охлаждении до комнатной температуры a-кристаллы изменяют состав в направлении от точки x4 к точке x2 вдоль кривой, а вторичные P-кристаллы изгибаются соответственно в направлении от точки z3z4 к точке z4. 126*2-ty3 аналогичная стадия: W2-y3 — — — — — — — >Ah-2(первичная кристаллизация) * Uz~ * comn и I2-x4———* Pz3-z4 (вторичная кристаллизация). На кривой охлаждения
сплав 2 имеет две важные точки(см. диаграмму. 71). В структуре из сплава 1 (см. схему. 12) отличается только тем, что имеет несколько больше вторичных Р-кристаллов(2×4/x4z4>>1×2 / x2z2) и соответственно меньше первичных а-кристаллов (2z4 / x4z4< Аналогичное превращение происходит в области BDD сплава. В этих сплавах первичные Р-кристаллы выпадают из жидкости, а вторичные а-кристаллы выпадают из них в твердом состоянии. В сплавах в области Abdc, помимо первичных кристаллов a или p, различают эвтектические a+p, а в твердом состоянии-различные вторичные кристаллы. Первичная кристаллизация сплава
3 из области AET e2c(рис. 70, Б»» * U6 может быть написано как ЖЗУБ > aXs_x<Е2, как только жидкость приобретает состав точки линии U6 на эвтектической кривой е Т6 (и максимум кривой растворимости в точке Х6 от сети переменного тока), таким образом, кристаллизация со-В+Р На данный момент в состав сплава 3 начинается. Состав первого Эвтектического Кристалла p, выпадающего из раствора JUB вместе с Кристаллом AHB, представлен точкой z6, которая расположена на второй кривой
максимальной растворимости bd. Начальная стадия кристаллизации сплава 3 эвтектика a + p может быть записана 1U6 как JUB — — — >aXfc+P2B, и равновесие этих фаз, в этой точке, рисуют первый соузловой треугольник x6y6z6, метафорическая точка сплава все еще находится в его малом аспекте x6u6, указывая на равновесие первичного AHB и оставшихся жидких jabs. Долю этих фаз можно оценить по соотношению сегментов Zu6/x6u6 и Zh6 / x6u6. Поскольку двойная эвтектика в тройном сплаве должна кристаллизоваться в интервале температур (B=K-f)+ 1 = 3 — 3 + 1 = 1 ), затем, по-видимому, при дальнейшем понижении температуры состав
кристаллизационной жидкости изменяется в направлении от точки y6 к точке y8 вдоль эвтектической кривой ehe2, а состав a-и p-кристаллов изменяется.、 Заключительную стадию кристаллизации сплава 3 эвтектики а+р можно записать в равновесие Жу б — — — — > АХБ+Пзб>и исчезнувших жидких Жув-и П2Б-кристаллов, в точке которого рисуется последний конический треугольник-127-х^гзг, его большие стороны х^АХЭ-и [характеризуют равновесие [кристаллов^ ^ гзг] проходит метафорическая точка сплава, и последний след жидкости должен исчезнуть внутри него. Были определены фазовые равновесия в начале и конце кристаллизации co-A+p, а также треугольные x по 6z6 и XB^b, которые отслеживают изменение соотношения различных фаз сплава при кристаллизации эвтектики a+λ по треугольному центроидному правилу, что является дальнейшим развитием правил Леваля, связанных с трехфазными
сплавами. 72 изображает эвтектическое равновесие X1Ah,+PZ, другой треугольник x7y^z7? При промежуточных температурах f / 7 с интервалом эвтектической кристаллизации a+P, когда в сплавах 3 присутствуют все три фазы: P7 и pz?. Если три сегмента прочерчены через фигуративную точку сплава на пересечении с вершиной этого треугольника и другой стороной, используя соотношение сегментов 3m / my7, 3k / Ah-и p27-кристаллов в этом сплаве. По существу, метафорическая точка сплава 3 является центроидом массы его фазы, а регистрируемое отношение сегмента-механическим равновесным состоянием плоского плеча в виде треугольника x7y7z7. Райс, семьдесят два Закон центра тяжести треугольника подтверждает, что кристаллизация эвтектики a+p сплава 3 фактически заканчивается, когда жидкость принимает
состав точки y, в то время как A-и P-кристаллы являются большими сторонами точки X8 треугольника x ez8x^^z6 проходит через метафорическую точку сплава, и жидкий JUD должен умереть в точке 3. Доля остальных АХА-и P2B-кристаллов определяется соотношением сегментов 3z8/x8z8 и 3×8/x8z8. Следует отметить, что в конце кристаллизации эвтектики имеется конический треугольник x auvg b«, представляющий собой равновесие исчезающей жидкости JUD с aXfj-и P2B-кристаллами. На внешней стороне этого треугольника нарушается материальный баланс компонентов,
поэтому метафорической точки сплава 3 быть не может. Вследствие снижения взаимной растворимости компонентов в твердом состоянии при более низкой температуре состав кристаллов aXjJ-и P2B 128ne будет оставаться постоянным, а будет меняться в кривые XgX9 и Згз, размещенные соответственно в области ктпс т и b1bdd1. Все кристаллы AHE (первичные и эвтектические) вторичные 0 -, и охлаждение от кристаллов 0gv (эвтектического происхождения) до комнатной температуры, * XB^COMN_AS AHE_ — — — >pZe_Z9. При комнатной температуре все а-кристаллы (первичные, эвтектические и вторичные) принимают состав точки Х9 по изотерме растворимости, а р^а целые^кристаллы (эвтектически и вторичные)-соответственно изотермический (по кривой охлаждения), а в структуре-преимущественно три
структурных компонента: а-Кристалл, со-Кристалл,++0 и 0-Кристалл (см. диаграмму). 13). Подобно сплаву 3, сплав в области кристаллизуется с теми только различиями, вместо того, чтобы первичные a-кристаллы падали, 0-кристаллы падали, и вторичные a-кристаллы из первичных и эвтектических 0-кристаллов. В сплаве 4 расположена эвтектическая кривая e te2 (см. фиг. 70, Б), первичные А-или 0-кристаллы не изолированы. Кристаллизация этого сплава начинается с выделения эвтектики: W l_v——— «——- * и XM> — Chi+после его кристаллизации, как и в предыдущем сплаве 3, происходит вторичная кристаллизация: * HP » * COMN ax t l-x12g —
■>Pzu-в результате этот сплав имеет две важные точки На кривой охлаждения (см. диаграмму).. 71), а структура-главным образом один структурный компонент-эвтектика а+0(см. также статью 9). Сплав 3 и 4, различные структурные части делят можно определить используя правила рычага. На примере этих сплавов, мы видели(см. рис. 70, Б), процесс кристаллизации эвтектики а+0 рисуется коническим треугольником, который при понижении температуры движется по кривой AC и BD под углом»вперед». Другими словами, содержание компонентов в направлении, в котором движутся эти треугольники, должно быть больше, чем содержание тех же компонентов В А-и таллах в жидкости. С Брандтом, всегда с э-Крисом- 3. Изотермический участок рассматриваемой системы значительно сложнее аналогичного участка системы с непрерывным рядом
жидкого и твердого раствора (см. рисунок). 58)поэтому мы рекомендуем их постепенное строительство: а)построение изотермы поверхности жидкой фазы(т. е. следа горизонтального сечения среза поверхности начала кристаллизации границы и 0-раствора); б)построение изотермы поверхности твердой поверхности(Б) построение изотермы растворимости (т. е. следа поперечного сечения среза границы и 0-раствора). В зависимости от температуры плоскость изотермического сечения не может пересекать все эти поверхности, поэтому задача построения определенного сечения может быть проще, чем описано выше. Для построения изотермических секций 600 и 500 ° с используется проекция системы(рис. 73). При 600°C (см. рис. 73, А) o жидкая фаза и поверхность жидкофазного раствора 0 (область a e te 1 и bet e2)
E горизонтальная плоскость сечения пересекается вдоль Изотерм E^и e CO точка плавления e T, а также начало, след от поперечного сечения поверхности солидуса A-и 0 раствора (AASS и B- Поскольку горизонтальная плоскость рис 73 130°С не пересекается, то на плоскости изотермического креста нет других кривых или прямых линий. Когда температура падает до 500°C(см. рис. 73, б) на плоскости изотермического сечения, происходят значительные изменения. Liquidus и solidus изотермические us4 и Xe yd4 и zd^ограниченная двухфазная область W+a и W+P ограниченная liquidus изотермическая us4 и yd * жидкость новая трехфазная область W+A+p (конодический треугольник) появляется в сплаве, где AH-и P2-кристаллизованная жидкость Zhu cocurrent фиксируется. Наконец, появляется новая двухфазная область a+P, окруженная
изотермами растворимости a^x и bj?. Малые стороны XY и yz треугольника Кононова xyz представляют собой следы поперечного сечения, горизонтальная поверхность среза доминирует над поверхностью начала кристаллизации эвтектики A+R (область aexe2c и b e^C f), а поверхность поперечного сечения. Понятно, что следы от этих участков поверхности всегда прямые, потому что они конноды. Отмеченная особенность изотермического сечения при 500°С может быть получена в общем случае: трехфазная область изотермического сечения является прямой линией, то есть стороной соответствующего конодического треугольника. Кривые Xa2 и zb2 представляют собой следы от поперечного сечения поверхности сольвуса (области a1B1 и b^d D j соответственно). Начиная с точек x и z максимальной растворимости AC и bd полисурмы, эти изотермы являются точками A2 и B2 кривой сольвуса двойной системы A-B.
С изотермическим сечением 20°C легко представить, что будут представлены только следы от поперечного сечения поверхности двух решателей. Правильность построения изотермических сечений можно контролировать по правилам количества фаз в последовательных пространствах состояний и в этих пространствах (т. е. фазовых областях). Характер (кривизна) различных кривых в изотермическом сечении определяется характером соответствующей поверхности на диаграмме пространственного состояния (см. Рисунок). 68). Обычно изотермы поверхности жидкой фазы поворачиваются своими выпуклостями в сторону области жидкого раствора (например, кривые E XC2 и e^2 на рисунке). 73, а), а изотерма поверхности сольвазы-наоборот, в сторону 131областы
граничных a-и 3-растворов(например, кривые показаны на рис. xc5 и zd5, a2x и b2z. 73,6). Построенное изотермическое сечение характеризует фазовое равновесие в любом тройном сплаве. Например, при 500°C (см. 73, Б) сплав 1 является однофазным, состоящим из кристаллов а (их состав совпадает с составом сплава), а сплав 2 состоит из кристаллов х и 3z, доля которых делится на сегменты 4. Многотепловая секция, такая как изотермическая секция, многотепловая секция анализируемой системы может быть собрана с помощью проекции, но концентрация тепла может быть уменьшена. Чтобы избежать ошибок, мы также Строим секцию полировщика шаг за шагом. Основные этапы построения любого
полисармарного участка включают: а) разделение участков на отдельные участки с помощью характерных сплавов. Характерной особенностью сплава является пересечение линий разреза с проекциями различных кривых на плоскости концентрационного треугольника. В полигретой части такого сплава может и не быть, и эта стадия выпадет. Сплав в каждой выбранной области имеет свои особенности кристаллизации и кристаллизации в твердом состоянии(см. ниже); б) построение кривой ликвидуса (т. е. сечение перпендикулярной плоскости поверхности начала кристаллизации по границам поперечного сечения следа а-и 3-раствора); в) сплошная кривая (т. е. пересечение следа с поперечным сечением вертикальной плоскости растворимой переменной режущей поверхности компонента в твердом состоянии). Концентрация планшетный мульти отрезок линии- Если 132 треугольника не пересекают все области и их границы, то задача построения такого сечения упрощается естественным образом. Рекомендуемый подход иллюстрируется на примере построения полисармарного разреза АП
(рис. 74). Что ликвидус состоит из двух кривых a’3 и 3p, соответствующих температуре начала кристаллизации A-и γ-растворов(в областях a-3 и 3-p делаются разрезы, что твердые лучи этого сечения соответствуют температуре, при которой Солидус a’2 и 4RG-температура в конце кристаллизации A и P растворов и все три твердые кривые представляют собой след поперечного сечения соответствующей твердой кривой на пространственной диаграмме (область на плоскости треугольника плотности — AACC, BBD).、 Аналогично кривые 2 ′ 3 ′ и 3 ’4′ являются линейной поверхностью
начала кристаллизации эвтектики a+p, спроецированной на плоскость концентрационного треугольника в области AEG E2C и bet e2d. Обратите внимание, что точки 2′, 3 ’и 4′ в секции полировщика AP обычно находятся при разных температурах. В этом случае точки 2 ’и 3′ получают при одинаковой температуре, затем в области 2-3 следа от поперечного сечения прямой поверхности эвтектики А+Р начинают кристаллизацию, образуя эту прямую поверхность. Кривые 2 ′ 1 ’и 4’2 на сечении Ar проецируются на плоскость треугольника концентрации, соответственно, следы от сечения вертикальной плоскости поперечного сечения двух решателей и bddv объясняют, почему кривые 4’2 сольвуса для 2.- 133канчивается точка Р2 (на вертикальном двойном сплаве р) не под помещение, тем выше температура. Кривая ограниченной
растворимости компонента C в плоскости концентрационного треугольника B представлена отрезком ddv, где точка d-температура te i, а точка dt-температура помещения. Точка P2 на этой кривой (или в ординате сплава p, который является тем же самым) должна быть температурой выше комнатной температуры (менее 1B2). Все кривые ЗС разделе Multi-тепло гладкие и не имеют точек экстремума. Если вертикальная плоскость этого сечения проходит через один из коннодов, образующих линейную поверхность начала кристаллизации эвтектики а+0, то образуется кривая 2’3’(или поперечное сечение этой поверхности). Характер (кривизна) различных кривых многотермического поперечного сечения определяется характером соответствующей поверхности на диаграмме пространственного состояния (см. Рисунок). 68).
Многотермические сечения, как это иногда бывает, не следует выделять в структурном чертеже, то есть не в фазовом составе сплава, а в размещении их структурных компонентов. Показаны только те фазы, которые присутствуют в различных сплавах при различных температурах, и эти фазы могут быть частью различных структурных компонентов. Например, сечение 1-р сплавов (фиг. Первичный А-или 0-Кристалл, эвтектический а+0 и вторичный 0 — или а-Кристалл: 74, б) в твердом состоянии содержит две а-и 0-фазы, но разные структурные компоненты.
Смотрите также:
Методические указания по материаловедению
