Оглавление:


Метод Уилка.
Метод Уилка. Из уравнения диффузионного процесса, основанного на предположении Эйлинга (см. предыдущий раздел) и уравнении Эйнштейна-Стокса(KP-7), Уилк[1]заключил, что величина P, которую он назвал «коэффициентом диффузии», помогает в расчете коэффициента диффузии. О жидкости: т. (Привет-18) Где P коэффициент диффузии (град•сек) Kem2•spz). T-абсолютная температура. C-коэффициент динамической вязкости. В некоторых парах рассматриваемых веществ (диффузия и растворитель) коэффициент диффузии Р является функцией молярного объема, поэтому он практически не зависит от температуры.
Температура кипения диффузионного вещества (Um-величина, приблизительно пропорциональная объему диффузионной молекулы), а также зависит от типа растворителя. Уилк рассчитал значения коэффициента диффузии Р для многих веществ, которые не реагируют с растворителем и не диссоциируют на ионы, и показал, что точки, соответствующие одному и тому же растворителю, соответствующие разным веществам, укладываются в общую кривую в координатах Р-1 и диаграммах Умнкнп.
Каждая такая кривая характеризует определенное значение параметра Φ, которое называется «коэффициент растворителя» и представляет собой отношение кинетического коэффициента рассматриваемого растворителя и диффузии веществ одного и того же молярного объема 1 л в water. Людмила Фирмаль
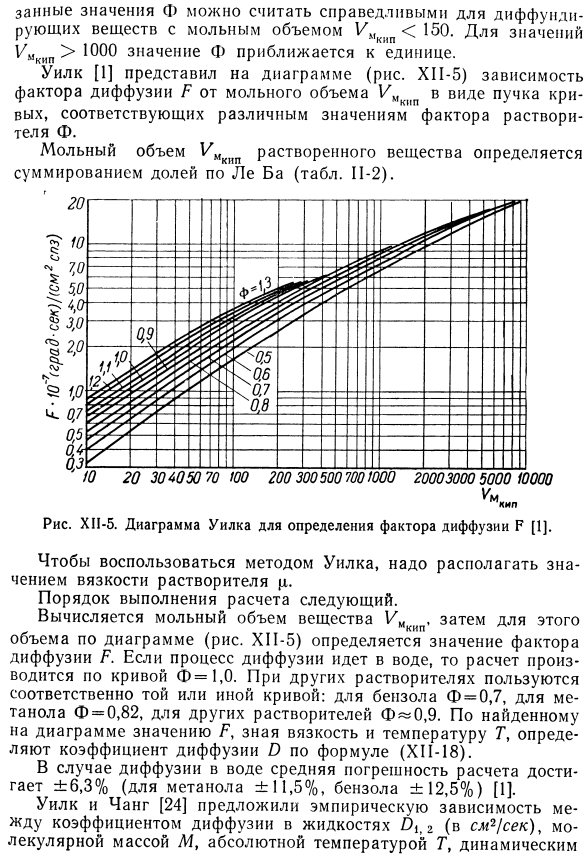
- In в случае воды коэффициент f = 1,0;в общем случае молярный объем растворителя, чем он меньше, тем он больше. Например, для бензола F = 0,70, для метанола F = 0,82.Значение Φ для других растворителей может быть рассчитано, когда известно хотя бы 1 экспериментальное значение известно. Примерно, можно взять Ф= 0.90.Постановление правительства Значение Φ можно считать эффективным при диффузии вещества с молярным объемом Y » <150.Для значений от 1/ m> 1000 значение Φ приближается к 1. Аппаратура Уилк [1] показал зависимость коэффициента диффузии P от молярного объема Vu в виде ряда кривых, соответствующих различным значениям коэффициента растворения F(рисунок CP-5). Определяется молярный объем растворенного вещества Общие доли по Le Ba(таблица N-2).
- Для использования метода wilc требуется вязкость растворителя p. Процедура расчета выглядит следующим образом: Рассчитайте молярный объем вещества Um и определите значение коэффициента диффузии P для этого объема из диаграммы (рисунок ХП-5).Если диффузионный процесс происходит в воде, то он рассчитывается по кривой кривой = 1.0.In другие растворители, 1 или другая кривая использованы, соответственно. Для бензола= = 0,7, для метанола= = 0,82, для других растворителей», 9 0,9.Из значений, приведенных на рисунке, вязкости вязания и температуры T, коэффициент диффузии O определяется по формуле (ср-18). В случае подводной диффузии средняя погрешность расчета достигает±6,3% (метанол ±11,5%, бензол ±12,5%) [1].
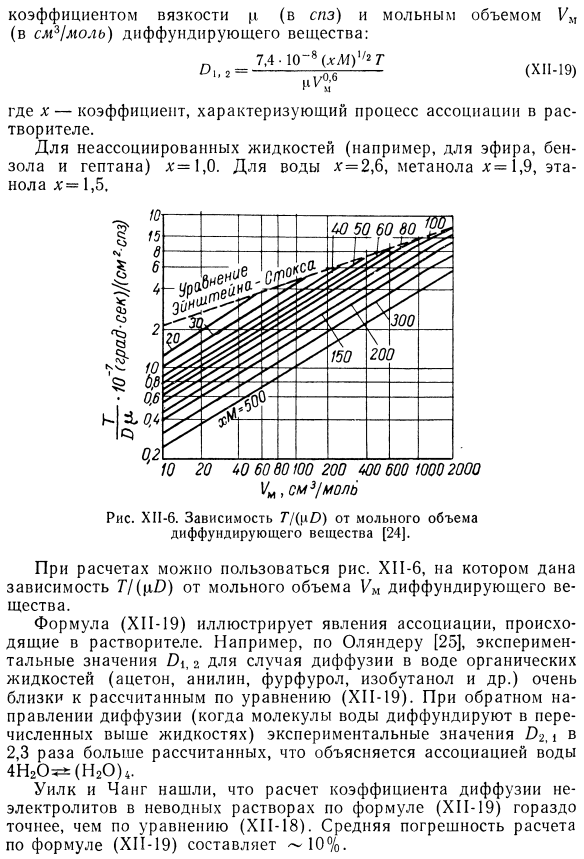
Уилк и Чанг [24]предложили эмпирические зависимости между молекулярной массой M, абсолютной температурой T, коэффициентом кинематической вязкости p(cc) и молярным объемом Um (см3 / моль) от 01,2 (см2 / с).Диффузионные материалы: (КП-19) Где Х-коэффициент, характеризующий процесс связывания в растворителе. Для жидкостей, которые не встречаются (эфир, бензол, гептан и др.), препарат равен 1,0.Для воды х = 2,6, метанола х = 1,9, этанола х = 1,5. Рисунок XII-зависимость 6.77 (cO) от молярного объема диффузного вещества[24].
При расчете можно использовать диаграмму. KP-6, которая дает зависимость от молярного объема диффузионного вещества. Формула (CP-19) показывает явление ассоциации, происходящее в растворителях. Например, по данным Оландера, экспериментальное значение 2 для подводной диффузии органических жидкостей (ацетона, анилина, фурфурола, изобутанола и др.) очень близок к рассчитанному по формуле (КП-19). Людмила Фирмаль
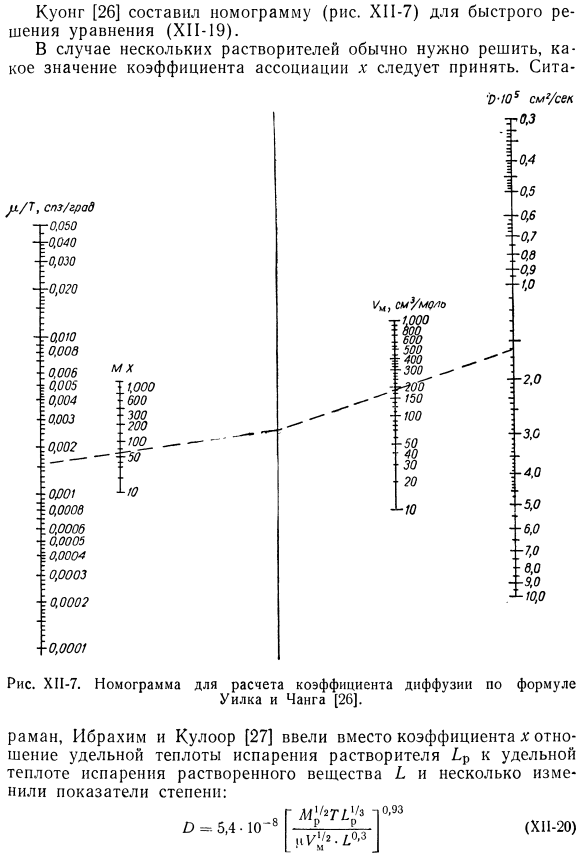
- Для обратной диффузии(где молекулы воды диффундируют в жидкости выше) экспериментальное значение 1 в 2,3 раза превышает расчетное значение. Это объясняется связыванием воды 4h20 ^(H20) 4. Уилк и Чанг установили, что расчет коэффициента диффузии неэлектролитов в неводных растворах по формуле (КП-19) значительно точнее, чем по формуле (XI1-18).Средняя погрешность расчета по формуле (КП-19) составляет около 10%. Куонг [26] отредактировал номограмму (рисунок XI1-7) для быстрого решения уравнения (KP-19). Обычно в случае некоторых solvents. It необходимо определить, какое значение V-связанного коэффициента следует принимать. Сита. Рисунок HP-7.Номограмма для расчета коэффициента диффузии по формуле Уилк и Чен[26]. Я…
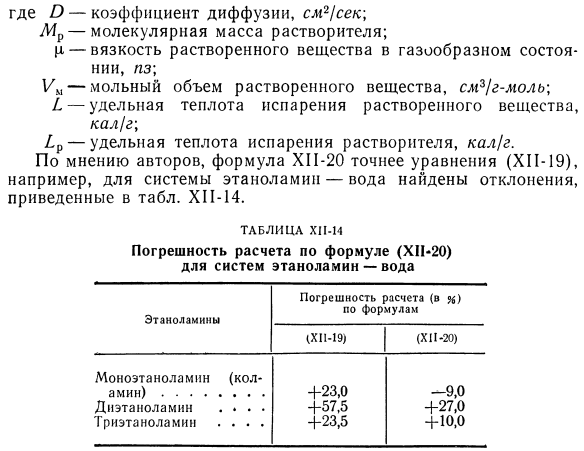
И некоторые изменения Раман, Ибрагим и Кулур [27]ввели отношение испарения растворителя Ap к удельной теплоте испарения Испарительная теплота растворенного вещества или индикатор степени; 。 Что?0,3^ (Привет-20) MU * PU41° ’ 93 О 5.4 −1(Г8 Где D-коэффициент диффузии, см2 / С. Mr-это молекулярная масса растворителя. В.-вязкость растворенных веществ в газообразном состоянии, ЛС; Yy-молярный объем растворенного вещества smg! Г-литераторы \ / , Удельная теплоемкость испарения растворенного вещества, кал / г; 1P-теплота испарения растворителя, кал / г По мнению автора, формула для HP-20 является более точной.
Смотрите также:
Методические указания по гидравлике
Возможно эти страницы вам будут полезны:
