Оглавление:






Общая характеристика металлов
- Общие свойства металла Из 106 известных в настоящее время элементов 76 являются металлами. Внутри таблицы. На рис. 1.Я… В ней показана периодическая система элементов Менделеева. Неметаллический элемент справа отделен толстой линией. Металлы в твердом и частично жидком состоянии обладают рядом характерных свойств.1) Высокая теплопроводность и электропроводность. 2) положительный температурный коэффициент электрического сопротивления; при повышении температуры увеличивается электрическое сопротивление чистых металлов.
Большое количество металлов(-30) обладают сверхпроводимостью (в этих металлах при температуре, близкой к абсолютному нулю, электрическое сопротивление резко падает, почти до нуля). 3) термоэмиссия, т. е. способность испускать электроны при нагревании. 4) хорошая отражательная способность: металл непрозрачен и имеет металлический блеск. 5) улучшать емкость пластической деформации.
Наличие этих свойств характеризует так называемое металлическое состояние вещества. Людмила Фирмаль
Все металлы и сплавы-кристаллические тела, атомы (ионы), атомы расположены в металле естественно, в отличие от аморфных тел, которые расположены хаотично. Металл(если он получен обычным способом)представляет собой поликристаллическое тело, состоящее из большого количества мелких (10-10-5 см) кристаллов, расположенных в разных направлениях друг от друга. Из-за условий кристаллизации они имеют неправильную форму и называются кристаллитами или зернами. Все наиболее характерные свойства металлов объясняются наличием легко движущихся коллокализованных электронов проводимости.
Атомы металла имеют небольшое количество электронов на внешнем энергетическом уровне. Связь внешнего электрона с атомом характеризуется работой функции электрона (или потенциала ионизации), то есть работой, необходимой для удаления электрона из изолированного атома. Если потенциал ионизации металла составляет от 4 до 9 эВ, то в неметаллах его значение обычно превышает 10 эВ при одиночной ионизации (то есть отсоединяется 1 электрон).Потенциал ионизации промежуточных элементов (Si, As, Se и др.) составляет 8-10 эВ. Эти данные свидетельствуют о том, что внешние электроны слабо прикреплены к ядру, поэтому они находятся в относительно свободном состоянии и образуют электронный газ. ФФ) Рисунок 1.
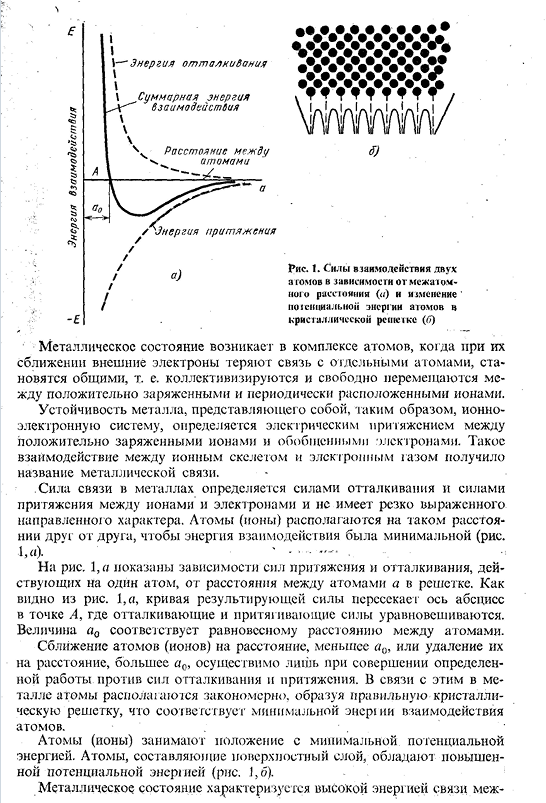
- Силы взаимодействия 2 атомов в зависимости от межатомного расстояния (а)и изменения потенциальной энергии атомов в кристаллической решетке (6) Состояние металла возникает, когда атомы сближаются друг с другом, а внешние электроны теряют контакт с отдельными атомами и становятся общими, то есть они свободно сталкиваются и перемещаются между положительно заряженными и периодически расположенными ионами. Стабильность металла, который является ионной электронной системой таким образом, определяется электрическим притяжением между положительно заряженными ионами и обобщенными электронами. Это взаимодействие между ионной структурой и электронным газом называется металлической связью. 。
Прочность связи металла определяется силой отталкивания и притяжения между ионами и электронами, при этом отсутствует ярко выраженная ориентация. Атомы(ионы) расположены на таком расстоянии друг от друга, что энергия взаимодействия минимальна (Рис.1, а). ’*■- >На рисунке 1А показана зависимость силы притяжения и отталкивания, действующих на 1 атом, от расстояния между атомами а в lattice. As как видно на рисунке 1А, результирующая силовая кривая пересекает горизонтальную ось в точке А, где силы отталкивания и притяжения уравновешены. Величина a0 соответствует равновесному расстоянию между атомами. приближение атома (Иона)на расстояние, меньшее А0, или удаление атома на расстояние, большее А0, возможно только в том случае, если была проделана
некоторая работа над силами отталкивания и attraction. Людмила Фирмаль
In в связи с этим атомы в металле располагаются естественным образом, образуя регулярный Кристалл lattice. It соответствует минимальной энергии взаимодействия атомов. Атомы (ионы) занимают позицию с минимальной потенциальной энергией. Атомы, составляющие поверхностный слой, обладают повышенной потенциальной энергией (рис.1.6). Металлическое состояние характеризуется высокой энергией связи между 9du атом. Его мерой является теплота сублимации, которая понимается как сумма энергии, необходимой для перехода конденсированной системы, то есть из твердого металла в парообразное состояние, Если атом больше не связан ионизацией energy. In в последнем случае они электрически нейтральны. / / теплота сублимации msgall варьируется в пределах 20220 ккал / (G-атом).
Приведенные выше положения позволяют объяснить свойства металла. Высокая электропроводность металлов объясняется наличием в решетке свободных электронов, движущихся в потенциальном поле. При повышении температуры колебания ионов (атомов) становятся сильными, и образуются вакансии、Электрическое потенциальное поле, препятствующее движению electrons. As в результате, электрическое сопротивление increases. At при низких температурах колебательное движение ионов (атомов) значительно уменьшается, что увеличивает электрическую conductivity. In у некоторых металлов в результате образования электронных пар, которые регулярно движутся при очень низких температурах (<20 к), электропроводность становится бесконечной-явление сверхпроводимости.
Высокая теплопроводность металлов обусловлена высокой подвижностью свободных электронов и, в меньшей степени, колебательным движением ионов. «Высокая пластичность металлов объясняется периодическим характером атомных структур и отсутствием направленности металла bonds. In процесс пластической деформации металлов(ковка, прокатка и др.), то есть при смещении их отдельных объемов относительно других объемов связи между ионами (атомами) не разрушаются. Если имеются ковалентные или ионно-связанные кристаллы, то есть направленные, то связь становится хрупкой, так как эта связь разрушается при деформации.
Известно, что электроны в атоме распределены по всей энергии level. In порядок увеличения энергии, эти уровни расположены в следующем порядке: is, 2s,3s, 3p, 3D,4s, 4p, 4d, 5s, 5p,5d, 4/, 6’s, 6p,7s, 6d, 5f. электронный вход уровня должен быть выполнен в том же порядке. Однако в металлах 4-6 периодов (от Sc до Ni, от V до Pd, от La до Pt и др.), 3d, 4d и 5D, 4F и 5 / ’уровни заполняются электронами только после следующего. Позади них, соответственно, уже 4, 5 и 6 секунд filled. An незавершенный D или / уровень металла называется металлом■ ’tn / h’.шдий-грш-оставшийся металл (или свободный d-уровень в случае металла с меньшим атомным номером), который полностью заполнен d или/уровнем, называется простым. 。
Металл переходной группы отличается от простого своим properties. An незаконченный внутренний электронный d-или/: уровень определяет свойства переходного металла: переменную валентность, парамагнетизм, ферромагнетизм некоторых элементов (Fe, Ni, Co и др.), высокая теплота сублимации и, следовательно, высокая температура плавления. Структурное состояние чистого металла 1 низкое » 1 понятие чистого металла очень conditional. In в будущем, под термином чистый металл, мы будем использовать металлы 99,99-99,999% purity. In во всех остальных случаях речь идет о технически чистом металле, содержащем небольшое количество примесей (99,5-99,9%), полученных обычным способом введения. 10. он применяется сравнительно редко, поскольку является прочностным и зачастую не обеспечивает необходимых характеристик.
Наиболее широко используется сплав. Сплав получают сплавлением или спеканием металлов с 2 или более металлическими порошками или неметаллами. Они обладают свойствами, присущими металлическому состоянию. Химические элементы, входящие в состав сплава, называются компонентами. Сплав состоит из 2 или более компонентов. В металловедении широко используются понятия системы, фазы и структуры. Ряд фаз, находящихся в равновесии, называется системой. Фазу называют однородной (гомогенной) составляющей системы, она имеет тот же состав, кристаллическую структуру и свойства, то же агрегатное состояние и отделена от остальных. Часть поверхностью раздела.
Под структурой понимают форму, размер и характер относительного положения соответствующей фазы металла или сплава. Структурным компонентом сплава называют изолированную часть сплава, которая имеет одинаковую структуру с характерными признаками. Различают макроструктуры(структура металла или сплава видна невооруженным глазом или незначительно увеличивается в 30-40 раз) и микроструктуры (структура металла или сплава наблюдается под микроскопом при большом увеличении). Макроструктура может быть изучена в трещинах и специальных макросечениях.
Изучение деструкции является наиболее простым способом обнаружения кристаллической структуры металлов (Рис.2, а).От трещин, размера частиц, характеристик плавки и литья(температура литья, скорость, равномерное охлаждение сплава и др.), термообработка, и поэтому о некоторых свойствах металла можно судить. Тип разрушения используется в качестве критерия при определении склонности к хрупкому разрушению стали. При исследовании макроструктуры специального макросечения (шаблона) образец вырезают из крупной заготовки (слитков, кованых изделий и др.) или изделие, поверхность которого полируют, полируют, травят с помощью специальных реагентов. Исследуя макросечение, можно определить форму и расположение зерен литого металла (рис. 2.6).
Кованые изделия Волокнистые (деформированные микрокристаллические)И. Дефекты, нарушающие непрерывность металла (усадочная хрупкость, пузырьки, оболочки, трещины и др.); химические неоднородности сплавов, вызванные процессом кристаллизации или созданные термическим или химическим нагревом (цемент, нитрид и др.) лечение. (Рисунок 3, a, b)Взаимное расположение фаз, формы и размеров. Для определения микроструктуры из небольшого образца исследуемого металла создается микрорез, то есть одна из его плоскостей тщательно шлифуется, полируется и травится специальными реагентами. Тонкая структура металла наблюдается в световой микроскопии или электронной микроскопии. 11 разрешающая способность оптического микроскопа, то есть минимальный размер объекта(детали конструкции)не превышает 0,2 мкм(2000 л), так как их можно различить с их помощью.
Полезное увеличение в световой микроскопии достигает 2000 раз. Потому что применение большого масштаба не помогает Фигура. 3.Микроструктура » — то же самое. techo (x 250); B-0,8% C сталь (x 300); C-0,8″ c сталь (электронный микрограф, x 5000) Электронный микроскоп I G использован обширно для того чтобы изучить микроструктуру, разрешение будет гораздо высокее, так, что 12kak без изменять сигнал только разрешит силу определенную природой волны света остает неизменно, которая приводит к в замечательной новой более точной детали структуры.
Использование электронного пучка имеет очень короткую длину волны [(0,04-0,12) 10-8 см], что позволяет детально изучить размеры объекта в 2-х его размерах, соответствующих расстоянию между атомами, т. е. 5 А… Наиболее широко используется трансмиссионный электромагнитный микроскоп, в котором поток электронов проходит через объект исследования. Полученное изображение является результатом неравномерного рассеяния электронов на объекте. С помощью электронного микроскопа можно детально изучить микроструктуру (субструктуру) металла.1. одним из важнейших результатов электронной микроскопии является непосредственное наблюдение структуры кристаллов defects.
In в электронном микроскопе (для предотвращения вторичного излучения, искажающего наблюдаемое изображение) часто исследуется не сам металл, а лак, полученный с поверхности вытравленного тонкого среза (или обрыва), или чаще углерод (или кварц), и оттиск самого металла ©, воспроизводящий детальную структуру изображения. Утверждение метода прямого исследования, широко used. In в этом случае исследуется тонкая пленка приблизительно 102А, которая получается из объемного образца, проходящего через электроны. 。
В последние годы все большее распространение получает растровый электронный микроскоп, и изображение создается вторичной эмиссией электронов, испускаемых с входящей поверхности потоком первичных электронов, непрерывно движущихся вдоль этой поверхности. ■ С помощью сканирующего микроскопа можно непосредственно исследовать поверхность (трещину) металла, но ее разрешение ниже, чем у просвечивающего электронного микроскопа (250-300 а).
Смотрите также:
Решения задач по материаловедению
