Оглавление:

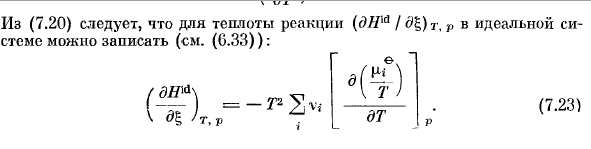


Парциальные мольные величины
- Частичное значение Моренос Мольталь. От(6.32) Т ИД. привет._ У’2. ^ Джей-РМИ в XI в Т Xi 1 dT J p. n. Р. С. С. dt.
Пожалуйста, сначала рассмотрите частичное продолжение Вт ч \ Т! \ Т! ДТ р, п от -Я и есть (7.20)
Используя определение(7.1), мы устанавливаем ключевые характеристики парциальной молярной массы в идеальной системе. Людмила Фирмаль
Это связано с тем, что член R в Xi не зависит от T. часть компонентов идеальной системы, так как она зависит только от T, молярная энтальпия не зависит от состава системы, она определяется только температурой и давлением.
- Часть компонентов идеальной системы молярного объема имеет те же характеристики. (7.21) Ах> «( =-*)、 ДП J Т (7.22)) С другой стороны, частичная молярная энтропия изменяется в соответствии с составом следующим образом. ? — (%- )- «И」 Из (7.20) будет получена теплота реакции (cWm / g£) m. P идеальной системы можно записать (см. (0.33))):
Аналогично из (7.21) и (0.34) получаем уравнение изменения объема реакции Tt (d ’/ dl) в идеальной системе
. Изменения громкости также не зависят от конфигурации системы. Наконец, частичная производная (dS /(U) m、 P идеальной системы (6.35) и может быть найден с помощью (7.22):
Теплота реакции в идеальной системе не зависит от концентрации, определяются только T и p. Людмила Фирмаль
Смотрите также:
| Идеальные системы и системы сравнения. Определение идеальных систем. | Сродство и однофазной идеальной системе |
| Уравнение для рц II | Химическое равновесие в идеальной системе |
