Оглавление:



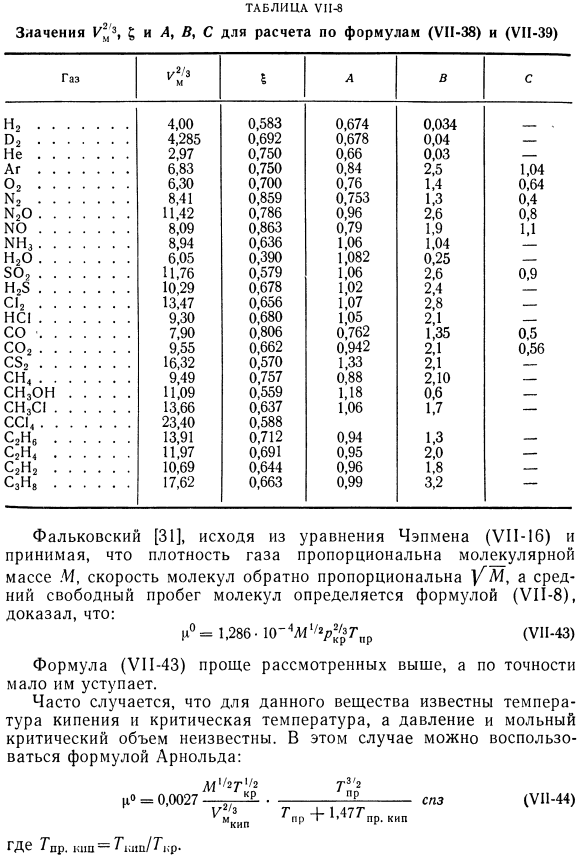


Полуэмпирические уравнения для расчета вязкости газов в области умеренных давлений.
Полуэмпирические уравнения для расчета вязкости газов в области умеренных давлений. Уравнения, полученные на основе кинетической теории газов (UN-15) или уравнений Чепмена(UP-16), редко используются для расчета динамического коэффициента вязкости газов. Ранее были приведены некоторые полуэмпирические уравнения для расчета вязкости Р, полученные с учетом сил взаимодействия молекул. Возможность применения уравнения (UP-22)-(UP-24) ограничена, когда известны определенные силы o и e (см. таблицу 1-16).Если у вас нет этих данных, то вам нужно воспользоваться эмпирической зависимостью-см. формулу-up-28.После преобразования получается полууравнение для вычисления значения вязкости газа p°. 2 полуэмпирические формулы (UP-30) и (U11-31) Бромли и Уилка уже были mentioned. In кроме того, учитываются уравнения, предложенные другими исследователями.
Если значение p не зависит от давления, то все формулы, приведенные в этом разделе, относятся к области среднего давления. Людмила Фирмаль
- Для определения зависимости коэффициента динамической вязкости газов от температуры в диапазоне средних давлений чаще всего используется формула Сазерленда. «О _» о 273.2 + ц / Т \ З / 2 ИГ-11°т + з \ 273.2 1 (ООН-36) Куда? м? Вязкость газа при температуре T°K; 0 вязкость газа при температуре 0°C; C-постоянная Сазерленда для конкретного газа. Значения i0.Уравнение Сазерленда(UP-36), например Таблица VI1-5 Сравнение расчетных и экспериментальных значений вязкости этилена| 1] Температура °С Значение динамического коэффициента вязкости этилена(микро товара) Обычно это дает точный результат сравнения таблиц. VI1-6 расчетных и экспериментальных значений вязкости этилена(Р2 = 96,13 мкпз\ с = 225,9). Фогель [26]доказал, что константа C может быть приблизительно вычислена из зависимости. С = 1,477 ′ Кипа. (До-37) Где Гипк-это температура кипения вещества, 0 К. Зависимости (UP-37) хорошо поддерживаются в Примере(вкладка UP-7).
- Чтобы использовать уравнения (UP-36) и (UP-37), необходимо знать вязкость газа при 1 произвольной температуре. Величина постоянной с практически не зависит от температуры. Например, для 0°СС= 113 воздуха, для 1600 ° СС = 124. Таблица VI1-7 Сравнение расчетной экспериментальной зависимости и температуры кипения констант Сазерленда Согласно уравнению Сазерленда (UP-Zb), вы получите более точные результаты, чем формула, предложенная в Reinganum, Trausem, energy equation и т. д. Риданд Шервуд [27] и гам-БПЛА [28]. Андрусовы [18, 29]предложили формулу для расчета вязкости газа.
Это означает, что если газ не соединяется и не разлагается,-50〜+ 1000 он имеет более высокую точность над диапазоном температур ° С (иногда до + 1600°С). (UI-38) 191,8 (\+U2M)/ Т \% 3636 1 273.2) Здесь / D. G-вязкость газа при температуре T(при умеренном давлении), pz * 10-6; M-молекулярная масса. / Поправочный коэффициент. Индекс; Um-молярный объем газа. Значение| / V2b можно вычислить, зная экспериментально определенную вязкость p. Индекс n (1 зависит от температуры (°C)): -A-B■KG4 / + S■KG7 / 2(UN-39) Внутри таблицы. UI-8 предоставляет значения, аналогичные L, B и C Несколько газов. О cr. 1 ~~ С » Р ТУ2 т | пр 1 пр \ ^ пр (ООН-40).
Лихт и Штехерт преобразовали уравнение Сазерленда, используя приведенные выше параметры. Людмила Фирмаль
- После замены Лихт и Штехерт получили следующую формулу: M1 / 2Pu * g3 / 2 со = * 0.000630 ^(ООН-42) P’R6 G » p + 0,8 Чтобы рассчитать кинематическую вязкость газа по формуле (UI-42), нужно знать только критические константы вещества (нужно рассчитать по формуле Бромли и Уилка). Стол-8 Значения для расчета по формулам (UN-38) и (UK-39) Y * ’ 3,$ n A, B, C На основании уравнения Фальковского[31], уравнения Чепмена (UN-16) и предположения, что плотность газа пропорциональна молекулярной массе M, скорость молекулы обратно пропорциональна CM, а средний свободный путь молекулы определяется по формуле (U11-8). И°= 1.286 * 10-4М Трансальп * Ltpr(ООН-43) Формула (U11-43) проще рассмотренной выше, но имеет меньшую точность. м * = 0.0027 М ’ ТЗ * У2> б ТГ> 2 1 Пр T’PR + 1.477СДР. (ООН-44) ав. Кипа.
Для некоторых веществ известны температура кипения и критическая температура, а также давление и молярный критический объем. unknown. In в этом случае можно использовать выражение Арнольд. Куда? Т’пр. Кипа. Формула (UN-44) менее точна, чем предыдущая. Флинн и Тодос [33]и стиль и Тодос [18, 34] нашли несколько формул, пригодных для расчета вязкости с относительно высокой точностью после расчета вязкости многих газов и анализа результатов. Они, для всех газов, содержащих неполярные молекулы, кроме водорода и гелия.
Смотрите также:
Возможно эти страницы вам будут полезны:
- оретический расчет вязкости газов с учетом сил взаимодействия молекул.
- Экспериментальные значения вязкости газов.
- Применение правила линейности для определения зависимости вязкости газа от температуры и давления; влияние состава газовой смеси.
- Расчеты вязкости газов, основанные на уравнении состояния реального газа.
