Оглавление:






Результаты измерении кинематического коэффициента диффузии в жидкостях.
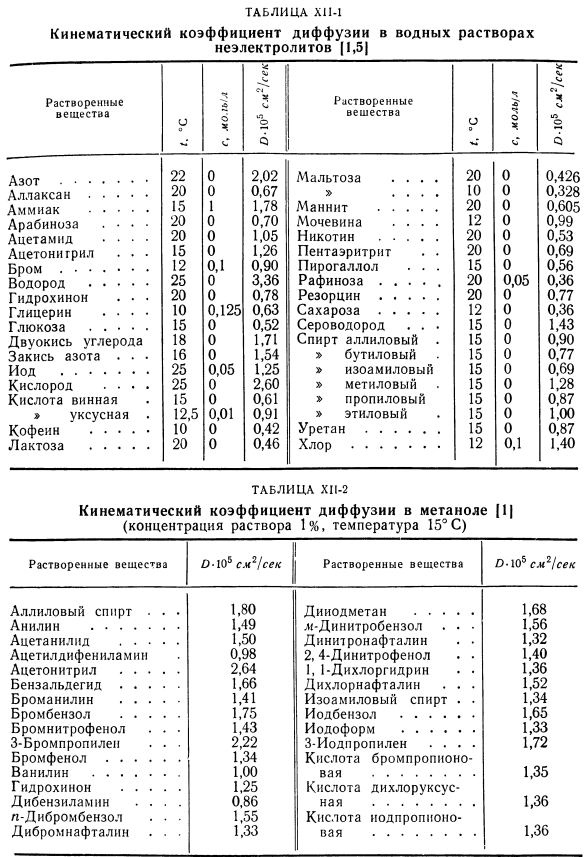
Результаты измерении кинематического коэффициента диффузии в жидкостях. Процесс диффузии жидкости во много раз медленнее, чем процесс диффузии газа. В случае жидкостей величина кинематического коэффициента диффузии D, которая определяется как в газовой фазе, по законам Фика (см. уравнения (Х1-7) и (Х1-8)), в 104-105 раз меньше величины коэффициента диффузии газа. Таким образом, кинематическая Коэффициент диффузии жидкой фазы может быть выражен не в см2 / с, а в см2 /сут. Преобразование использует следующие пропорции: I см2 (второй = 86,400 см7 [Солнце При изучении диффузионных процессов в жидкостях растворы электролитов следует учитывать индивидуально. Это связано с тем, что через него диффундируют ионы, а затем и молекулы. Жидкие системы, изучение диффузии которых имеет большое практическое значение, делятся на группы: неэлектролитные растворы, растворы электролитов, расплавленные соли, расплавленный металл и др. Выше приведена таблица значений коэффициента кинематической диффузии некоторых неэлектролитов и других типичных систем.
Экспериментально установлено, что кинематический коэффициент диффузии жидкости зависит от концентрации и температуры этих веществ. Таким образом, в таблице приведены значения коэффициента диффузии различных концентраций и температуры процесса диффузоров c в растворе. Людмила Фирмаль
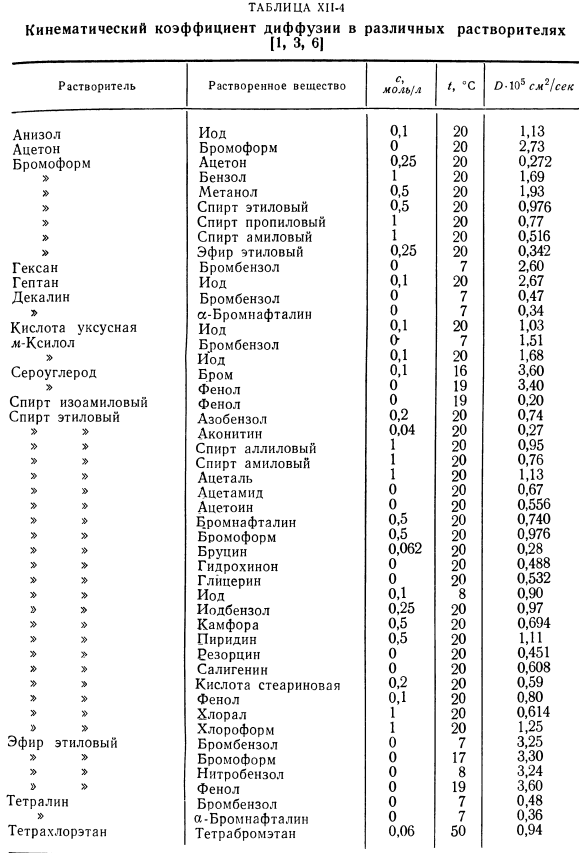
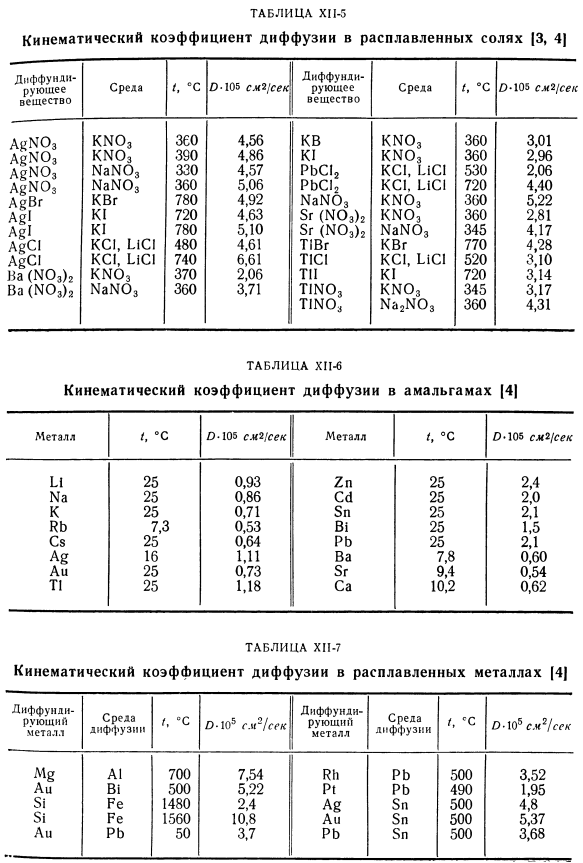
- XIM показывает значение кинематического коэффициента диффузии неэлектролитов в водной среде solutions. In таблица XP-2, значения динамического коэффициента коэффициента диффузии веществ, растворенных в метаноле, приведены в таблице XP-3 бункеров: зола, таблица CP-4-в других растворителях. Данные приведены в таблице. ХН-1-ХП-4.It в основном взят из исследования wilc[1] и дополнен результатами других исследований[2-6].Они в основном связаны с органическими веществами. Для характеристики диффузионного процесса других жидких систем приведены значения кинематических коэффициентов диффузии расплавленных солей (таблица СР-5) и амальгамов (таблица Ср-6).
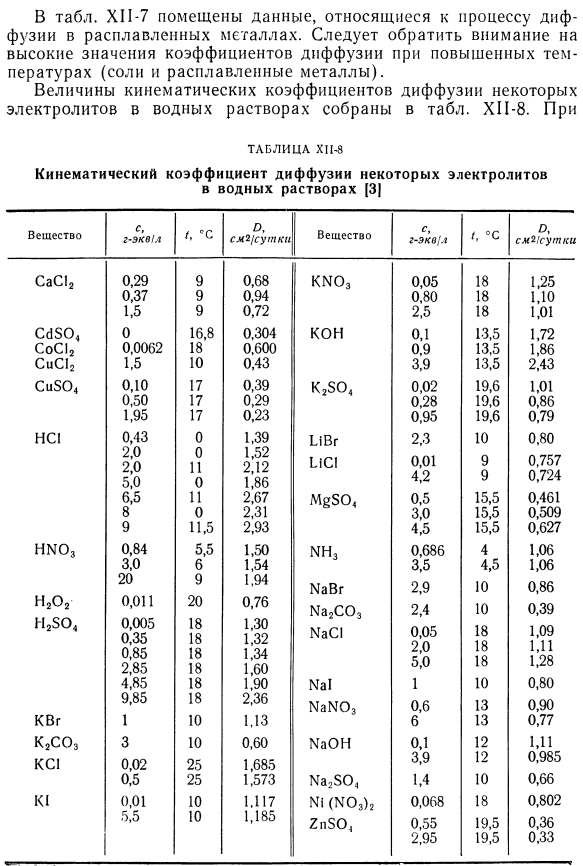
Внутри таблицы. CI-7 содержит данные о диффузионном процессе расплава metal. It следует отметить высокое значение коэффициента диффузии при высоких температурах (соль и расплавленный металл). Кинематические коэффициенты диффузии некоторых электролитов в водных растворах сведены в таблицу. Привет-8.Так… Таблица XI1-8 Если сравнить данные в этой таблице, то с увеличением концентрации величина и может увеличиваться или уменьшаться (в случае неэлектролитов она будет только уменьшаться).
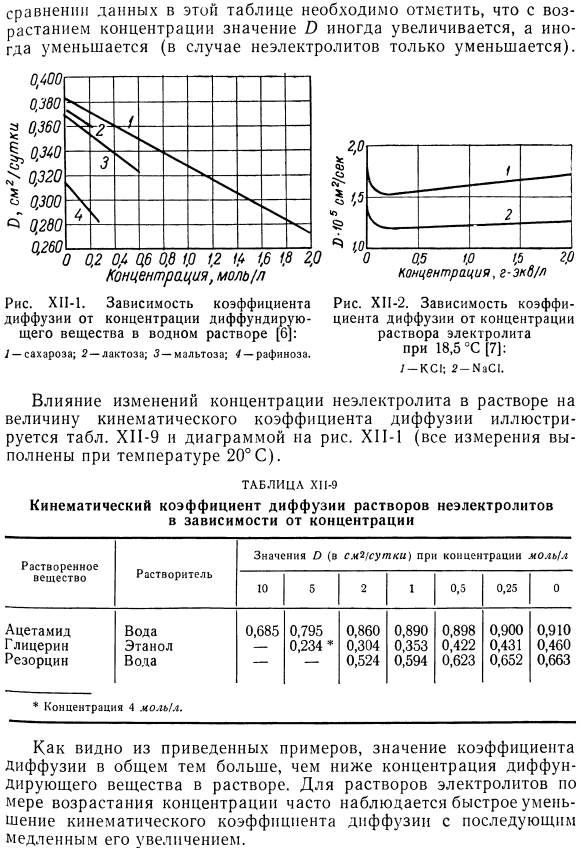
- Рисунок X11-1.Зависимость коэффициента диффузии от концентрации диффузоров в водном растворе[b |: Влияние изменения концентрации неэлектролита в растворе на величину коэффициента кинематической диффузии показано в таблице. Рисунок HP-9 n рисунок XI1-1(Все измерения проводились при температуре 20°C). * 4 молярная концентрация. Как видно из приведенного выше примера, в целом значение коэффициента диффузии увеличивается с уменьшением концентрации диффузоров в solution.
In в случае растворов электролитов при увеличении концентрации часто наблюдается резкое снижение коэффициента кинематической диффузии, который затем медленно возрастает. На рис. XI1-2 приведены данные для водных растворов хлорида калия и натрия при температурах 18,5°С. При повышении температуры процесс диффузии ускоряется. Чем выше температура, тем больше кинематический коэффициент диффузии. Например, Коэн и Брюинс [8] получили следующую температурную зависимость коэффициента кинематической диффузии b (при диффузии очень разбавленного раствора тетрабромметана в симметричном тетрахлорэтане, используемом в качестве растворителя).: °С 0.44 7.70 25.00 25.00 35.61 51.10 Ах, см2 / день. 。 0.303 0.362 0.429 0.528 0.640 0, (25 .
В данном примере при повышении температуры примерно на 50°с коэффициент кинематической диффузии увеличивается более чем в 2,5 раза. Людмила Фирмаль
- В узком температурном диапазоне практически можно принять линейную зависимость коэффициента диффузии O от температуры I. <X1I> Для ряда веществ с ^ = 10°С и^ −20°С значение а находилось в диапазоне от 0,03 до 0,04, и во многих случаях было установлено, что его можно вычислить по следующей формуле: а = 0.026-0.0211 ^ 0 (СР-2) Зависимости (XII-1) и (CP-2) являются эмпирическими. Из сравнения, приведенного в таблице. Данные CP-1-CP-8 показывают, что коэффициенты разных различных диффузоров в одном конкретном растворителе существенно различаются.
Точно так же большие расхождения наблюдаются, когда одно конкретное вещество диффундирует в разные растворители при одной и той же температуре. Например, Миллер [9]исследовал диффузию йода в различных растворителях при 20°C и нашел следующее значение O(единицы cmUsec). Бензол, 1,670 Бромбенон 1.388 Гептан 2,386. Метанол, 1,572. Углерода disulfide2, 697 4 ′ хлорированный углерод…. 1.177 этилацетат 1.859 Влияние давления на процесс диффузии будет заметно только при очень высоком давлении(более нескольких десятков атмосфер).Этот эффект характеризует зависимость Op / O0 от давления p. где 0P и A) равны.
Смотрите также:
Методические указания по гидравлике
Возможно эти страницы вам будут полезны:
