Оглавление:



Свойства кислорода
- Природа кислорода Физические характеристики. Кислород-бесцветный газ, не имеет вкуса или запаха, слабо растворим в воде (3,1 объема кислорода при 20 ° С, растворим в 100 объемах воды).
- Кислород немного тяжелее воздуха(1 литр кислорода в нормальных условиях-1 РНС. 22. Искусство. Или I атм = 0,1 МПа. Сито 1,43 г, 1 л воздуха-1,29 г). при нормальном давлении и температуре −183 ° Коксиген разжижается, а при понижении температуры до −218,8°С он затвердевает. Химическое свойство.
Горение фосфора под колоколом. 1 нормальное состояние (сокращенно: нет) — температура 0 ° С и давлении 760 мм рт. Людмила Фирмаль
Кислород бурно реагирует со многими веществами, выделяя тепло и свет. Такая реакция называется реакцией горения. Сущность реакции горения веществ в кислороде может быть определена экспериментально. Например, фосфор сжигается под колоколом (рис. 22).При горении в колоколе поднимается вода, за счет чего в воздухе расходуется кислород.
Когда тлеющие угольки опускают в емкость с кислородом, он горит с огнем. incandescence. To определив, какое вещество образовалось, известковую воду заливают в емкость. При сгорании углерода образуется монооксид углерода (IV), который создает облачность. Иви. С + 02 СО2 Диоксид углерода Углерод (IV)) Сера горит кислородом ярким синим пламенем с образованием газа с резким запахом-оксида серы (IV): ИЖ ВТОРОЙ с + О2 ѕо2 Сера, кислород, оксид. Сера (IV) Фосфор Р горит с кислородом в ярком пламени: 4P + 502 2P2Ob Фосфор оксид кислорода Линн(В))
В кислороде сжигаются такие вещества, как железо, которые обычно считаются негорючими. Если прикрепить спичку к тонкой стальной проволоке, поджечь ее и положить в емкость с кислородом, то железо тоже загорится от спички. Горение железа происходит при рассеянии трещин и ярких искр-расплавленных капель оксида железа Fe304 в этом соединении 2 атома железа имеют 3-валентность, 1 из них-2-валентность.
- Таким образом, реакция горения железа в кислороде может быть выражена следующей формулой: Привет. 3Fe + 202 FeO * Fe203(или Fe304) Оксид железа Oxidation. In оксидная химия, вместо выражения «вещество горит», чаще всего используется фраза » вещество окисляется*» used. As мы увидим позже, что понятие «окисление»более распространено, чем понятие»горение».Суть процесса окисления описана на 132 страницах.
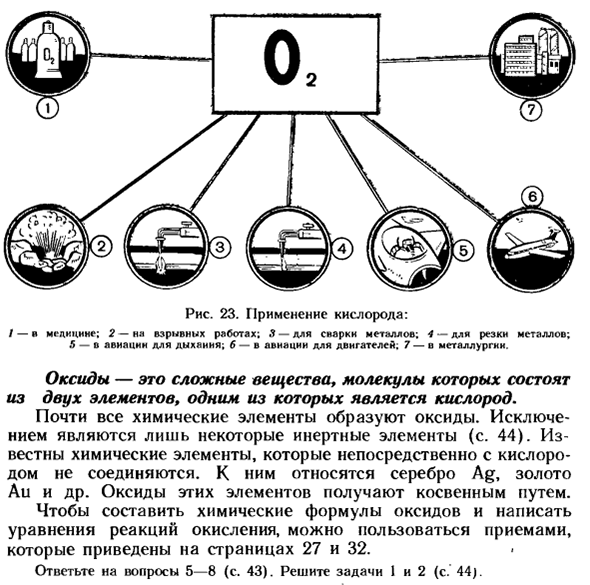
Взаимодействие кислорода с веществами относится к окислению reaction. 23.Использование кислорода: — Я-наркотик. 2-во время взрыва. 8-для сварки металлов; 4-для резки металлов. 5-авиация для дыхания. Ъ-двигатель авиации. 7-в металлургии. Оксиды-это сложные вещества, молекулы которых состоят из 2 элементов, 1 из которых-кислород.
As в результате взаимодействия веществ и кислорода образуются различные оксиды. Людмила Фирмаль
Почти все химические элементы образуют оксиды. Единственным исключением являются некоторые инертные элементы(стр. 44).Известны химические элементы, которые не связываются непосредственно с кислородом. К ним относятся серебро, Au-золото и другие. Оксиды этих элементов получают опосредованно.
Для составления химической формулы оксида и описания уравнения реакции окисления можно использовать методы, описанные на стр. 27 и стр. 32. Вопрос 5-8 (стр. 43).Решите задачи 1 и 2(стр. 44j.
Смотрите также:
| Кислород, его общая характеристика и нахождение в природе | Применение кислорода |
| Получение кислорода | Воздух и его состав |
Если вам потребуется заказать решение по химии вы всегда можете написать мне в whatsapp.
