Оглавление:








Типы диаграмм состояния
- Тип диаграммы состояния. Построение диаграмм состояний и их геометрия Химический анализ при изучении химических превращений в системе Основная задача физико-химического анализа — наиболее мощный и、 Универсальный метод современной химии. Для графических изображений
- Состояние однокомпонентной системы, 2 координаты p и T достаточны(плоские Кости), потому что ее состав фиксирован. 2 определить состояние ингредиентов Система сущностей по 4 параметрам основанная на равенстве f (p, T, x\, xr) −0, достаточно знать 3 из них: температуру, давление, концентрацию Тяга любого компонента. Удобно представить конфигурацию системы в виде отрезка с длиной Он принимается в качестве unit.
Когда мы рассматриваем соотношение между молярной долей ингредиентов (x \ 4 — x2 = 1) Людмила Фирмаль
In кроме того, его конец 1 является чистым com- Еще одна из записей a (t = 1, x2 = 0), чистая составляющая B (x \ = 0, x2 = 1).И затем… Средняя конфигурация характеризуется точками на этом segment. So … Точки M 92 на рисунке, фракция B равна 0,35, фракция A равна 0,65(или 35%B и 65%A). Значения внешних параметров P и T в этой системе координат полезны. Ударьте в 2-х направлениях перпендикулярно друг другу. В некоторых случаях объяснить систему конденсации、
Давление не влияет на положение равновесия. Затем, когда вы получаете P = const,、 Возможность отображения состояния бинарной системы на плоскости( Максимальная Т-Х)(рис. 93).Любая фигуративная точка в этой сетке* M P = const однозначно характеризует состояние system. To построить На диаграмме T-rf исследуется температурная зависимость времени охлаждения Расплавы различного состава.
Полученная таким образом температурная кривая имеет вид * Точка, отражающая состояние системы, называется отношением фиг、 Координаты равны значениям параметров. 1J4 Время P и s. 94.Кривая охлаждения Это время называется кривой охлаждения. Эти типы T-1 g Кривая указывает на наличие или отсутствие Специфическое специфическое преобразование участка Температура или диапазон температур(рис. 94).
В соответствии с 3 возможностями Тип равновесия (Ди -, моно -, инвариантный) Наблюдаются 3 различные кривые охлаждения. Кривая 1 соответствует охлаждению образца без его охлаждения Вторая фаза преобразования. Кривая 2 отражает моно Вариант процесса, который происходит с интервалами Температура ТН-ТК. Кривая 3 не является Созревает процесс, при котором температура должна поддерживаться постоянной.
Кривая охлаждения останавливается при температуре、 Растворение чистых компонентов, соединений постоянного состава В случае стехиометрического расплава (Р = const), с точки зрения фазового правила Система также является 1 компонентом(C = 1 + 1-2 = 0).Также、 Кристаллизация и мощность 2-х бинарных компонентов Степени свободы также равны нулю: K = 2, Ф= 3(2 твердожидкие фазы) и С= = 2 + 1-3 = 0).Другое равновесие должно быть неизменным. Если бинарная система имеет 3 фазы.
С характерным поворотом Остановка Т-3 ^кривая охлаждения сплавов различного состава- Состояние ГЛ. В зависимости от особенностей взаимодействия компонентов Существуют различные типы диаграмм состояния. Наиболее распространенная система, в которой компоненты не ограничены Смешивают в жидком состоянии(полная взаимная растворимость).
Случай Этот компонент совершенно неразрешим в твердом состоянии друг к другу и、 Не образуются химические соединения, это отражено на диаграмме состояния Эвтектического типа (рис. 95).Из закона идеальных решений( Osprey), когда вы добавляете 2-ой компонент, точка плавления пойдет вниз Фогт. Рассмотрим процесс кристаллизации сплавов. Его состав показан на рисунке 1.95 каждый Пункт 1 Правила.
Точка сравнения В области жидкой фазы L фазовый переход системы не происходил Дочернее равновесие будет двумерным*(C = 2 + 1-1 = 2).Падение температуры Когда расплав охлаждается, он происходит по гладкой кривой. Когда вы достигнете Отношение кривой Т Е при температуре точки Т фиг, расплав насыщается Для компонента а, где кристаллы начинают осаждаться из расплава Далее уменьшите температуру. За то, что Из-за высокой температуры кристаллизации при охлаждении появляется излом curve. So … Способ, при котором из расплава первоначально выделяется только компонент а, жидкая фаза Ингредиент в концентрируется.
Когда температура падает в равновесии、 Кристаллы компонента А содержат жидкую фазу различного состава. Тенденция к точке Е вдоль кривой ТЕ. Количество степеней свободы в этом случае А. ’ Равно единице (C = 2 + 1-2 = 1). * P-вариация системы в const является условной. Истинная вариация на единицу Больше. Как только система охлаждается до температуры te, расплав насыщается И связанные с компонентом В. Следовательно, в будущем, в то же время Оба компонента кристаллизуются:
Где L-жидкость. S и S-составные кристаллы. Состав расплава Ответьте на точку е на диаграмме, не меняя ее. Максимальное число фаз, число степеней свободы C = 2 + 1-3 = 0, и эквивалент Это и есть immutable. In кривая охлаждения, горизонтальная нью-йоркский заговор. Как только кристаллизация будет завершена, кривая охлаждения снова станет гладкой Уменьшение (C = 2 + 1-2 = 1).
Кристаллизация также продолжается. Все сплавы, состав которых на диаграмме состояния находится слева от точки Е Отверждение сплава, состав которого находится справа от точки Е (точка 3) Начиная с разделения кристаллов компонента В. жидкая фаза концентрируется Ингредиент А. процесс заканчивается обеими кристаллизациями Components. In кривая охлаждения 2, показана только горизонтальная область.
При такой температуре расплав сразу охлаждают. Насыщенный для 2 компонентов, чтобы кристаллизоваться вместе (C = 2 + 1-3 = 0). на диаграмме состояния кривые T E и T E называются Ликвидус. Они представляют собой геометрическое расположение точек, соответствующих Начальная температура кристаллизации. Обе линии сходятся в точке E. Называется эвтектика. Сплав, состав которого соответствует этой точке, является Плавление (плавление) при определенной минимальной температуре конкретной системы) Это называется эвтектика*.
Горизонтальная линия TP соответствие Температура Tg называется эвтектической горизонтальной. Она является геометрическим Сто девяносто шесть * Эвтектика, в переводе с греческого, означает «легко растворимый». ^ 4 + −4— Конфигурация Время Шесть Рисунок 96.Диаграмма состояния с неограниченными твердыми телами Вор (а) и кривая охлаждения(б) Место точки, соответствующей концу кристаллизации всех промежуточных продуктов Сплав в системе.
Потому что чистые ингредиенты а и в кристаллизуются Над эвтектической горизонталью (температура T, T соответственно)、 Солидус, где только твердая фаза существует ниже、 Закрыт жидкой фазой при температуре плавления Комплектующие. Рассмотрим случай, когда ингредиенты растворяются бесконечно Друг друга как в жидком, так и в твердом состоянии. Диаграмма 96 а Аграмы в состоянии таких систем.
Потому что образуется только охлаждение 1 твердая фаза переменного состава, Рис. 2 непрерывная Линия, соответствующая температуре начала и конца (Ликвидус и Солидус) Твердый раствор затвердевает a (P).Либо точка (но、 Tav) соответствует чистым компонентам) система не должна быть неизменной. Так как минимальное число степеней свободы равно C = 2 + 1-2 = 1、 Кристаллизация всех промежуточных расплавов не происходит в следующих случаях:
Температура, и в пределах некоторого диапазона температур. О кривой охлаждения Показаны 2 поворота, соответствующие началу и концу преобразования (рис. 96, 6). При образовании сплошного твердого раствора система встречается в следующих случаях Ликвидус и Солидус имеют общие точки соприкосновения и проходят через них Экстремум-минимум или максимум(рис.97, А, Б).Дополнительный По крайней мере, существует инвариантная настройка на кривой охлаждения.
Это вроде бы противоречит закону*. на самом деле、 В уравнении фазового правила необходимо учитывать дополнительное условие x ^ = Xg. Как правило, a обозначает твердое решение на основе компонента A и символ Лом Р-твердый раствор на основе компонента В. непрерывное формирование ряда Твердому раствору все равно, какой компонент считать растворителем. В обозначении a (/7). ** Равновесие двух фаз бинарной системы должно быть одномерным. С= 2 + + 1-2 = 1. Изменение системы на единицу. Традиционно такие системы можно рассматривать 1 компонент, то C = 1 + 1-2 = 0 Рассмотрены типы диаграмм состояния limited.
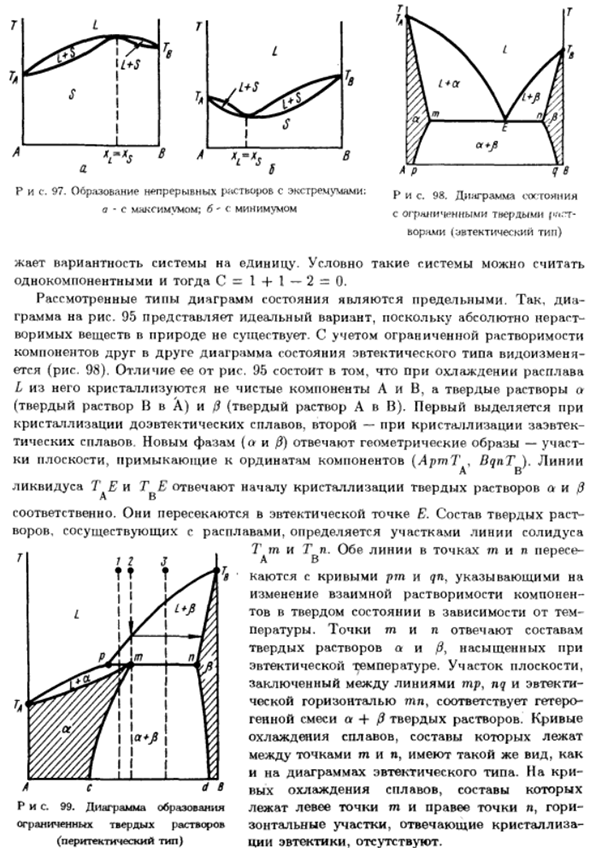
So, Диа- Рисунок G 95 представляет собой идеальный вариант. В природе нет воров. Подумайте об ограниченной растворимости Компонент, фазовая диаграмма которого эвтектического типа изменяется друг с другом- Вот это (рис. 98).Разница между рис 95 при охлаждении плавится Л из него кристаллизуется твердый раствор а, не чистые компоненты а и в (Твердый раствор B) и/или? (В твердом растворе а). в первом случае、 Кристаллизация переутектического сплава, при кристаллизации второго и переутектического Сплав.
Новые фазы (o и/) соответствуют геометрическим изображениям- Плоскость ki, примыкающая к ординате компонента (ApntT, BqnT).Ряд Линии Ликвидуса T E и T E соответствуют началу кристаллизации твердого раствора ai /) А б Accordingly. It пересекается в эвтектической точке E. состав твердых тел Вор сосуществует с расплавленной проволокой, определенной в секции Солидуса T m и T p. обе линии точек А б покайтесь на кривой, указанной pm и qn Изменение взаимной растворимости компонентов Твердое тело в состоянии, в зависимости от пература.
Точка типа соответствует соединению Твердого раствора АИ /?Насыщенный с Эвтектическая температура. Площадь участка Выводы между рядами tr, nq и эвтектика Горизонтальный TP, гетеро-совместимый Генная смесь а + /?Твердый раствор. Кривая Состав следующих охлаждающих сплавов Тип точка-точка, с тем же форматом, что и И диаграмма эвтектического типа. на CRE И его состав при d при охлаждении из сплава Рисунок 99.
Диаграмма формирования находится слева от точки m и справа от точки N. Ограниченный твердый раствор, пупочная область, соответствующая кристаллизации Нет эвтектические (эвтектика). 1Q8 Эвтектический горизонт, соответствующий инвариантному преобразованию Ниже температуры кристаллизации чистых компонентов А и в Система, в которой постоянная горизонталь находится между температурой и температурой Каркас кристаллизации компонентов.
- Такая горизонтальная линия называется перитектикой Ская. Этот тип диаграммы состояния показан на рисунке. 99.In эта цифра Вместо эвтектики происходит инвариантное перитектическое преобразование ниэ. Он состоит в растворении твердых кристаллов, которые ранее осажденный Вор/ 3 в расплаве определенного состава, в результате чего образуются кристаллы Для твердого раствора a: L(p) — f Dn)^^ a (m).Опыт подобных преобразований Во время охлаждения сплав, состав которого находится в пределах его диапазона Перитектический горизонтальный РП.
Если в системе образуется химическое соединение AmBn, то это означает Диаграмма состояния (рисунок 100).Эта цифра является официальной Лена-Ахв как комбинация 2 фаз эвтектического типа А AGOVP-B (см. Рисунок 98). Солидус представляет Накатал Т тугриков улучшенной конструкции. Соединение в диаграмме состояния В AtVp Б Соответствующее явному максимальному значению, соединение существует до температуры плавления Niya.
Линия Ликвидус состоит из 3 секций、 Начинается кристаллизация компонентов и соединений. Людмила Фирмаль
In в этом случае состав твердой и жидкой фаз при температуре плавления совпадает. Такое таяние называется кошерным энтонилом! (лат. от congruens-соответствующий), и Самая высокая температура кривой Ликвидуса называется distpektpika(от греч. «Трудно растаять»).Если соединение разлагается до достижения температуры На диаграмме состояния плавления нет явного максимума(рис. 101).
Новая строка PQ (перитектическая горизонталь), соответствующая не Константа равновесия: Aja » 5 = * L (P)+ S@); C = 2 + l-3 = 0. По смыслу он аналогичен перитектически-горизонтальному pn(см. Рисунок 99). Температура кристаллы TpAmBn разлагаются в соответствии с вышеизложенным Уравнение жидкости (рис. 101) в составе L (P) и твердого компонента s@). по Поскольку состав твердой и жидкой фаз не совпадает, это плавление является Ся непоследовательно (несообразно. НС-несоответствие).
Ликвидус состоит из 3-х частей Разветвление: T P-кристаллизация твердого раствора/?PE-твердый раствор Твердый раствор на основе соединения AmBn и т е. точка P называется / л Бег или конверт. Кривая EP представляет собой ряд пунктирных линий、 Метастабильный латентный максимум для определения виртуальной температуры Плавления соединения AmBn. Рассмотренными типами диаграмм состояния являются simplest. In факт Система взаимодействия описывается более сложными геометрическими комплексами Они сами представляют собой комбинацию этих types. As пример、
Просмотрите диаграмму состояния системы A1-Au (рис. 102). в этой системе、 Образуются 5 соединений: AuAl2, AuAl, Au2Al, Au5Al2, Au4Al.2 из них плавятся Согласно(AuAI2 и Au2AI), остаток образуется в результате перитектической реакции Можно также добавить, что 1 из этих соединений (Au4A1) образует твердую область Раствор 7-на основе золота, ограниченный твердый раствор является formed. In Твердый алюминий, золото практически нерастворим. Отсутствие заметного участка твердого раствора от A1.
In система Внимание к образованию 3 эвтектики Al + A2ual2, AuAl + Au2AI, Au5Al2 + + Au4Al. Геометрический анализ диаграмм состояний основан на 2 принципах: Н. С. сформулированный крнаковым-принцип непрерывности и Доказательства (корреляция).Согласно первому принципу, непрерывное изменение Состояние системы, индивидуальные фазовые свойства и Если система в целом тоже постоянно меняется, но не Новая фаза и старая фаза не исчезнут. Основанный на принципе непрерывности
Это возможно из анализа состава рисунка-определения числовых характеристик, характера фаз Системы, области их существования, особенности взаимодействия между ними. Принцип соответствия основан на каждой фазе, фазовом равновесии и Комплекс фаз соответствует геометрическому изображению диаграммы состояния. Фактически, на диаграмме состояния (рис. 103)、 Жидкая фаза соответствует области, ограниченной ординатой компонента、 200. Ликвидус (снизу).
Область твердого раствора на основе компонентов A, B и соединения AmBn и АжВу соответствуют замкнутым геометрическим комплексам a, p, 7, b, окруженные соответствующими линиями одномерного равновесия Вертикальная координата компонента. Кристаллизация каждого химического вещества Соответствует той части Ликвидуса (компонент A-T Ev соединен Atbn-E \ t \ P, соедините AjBu-PE2, компонент B-T E2).
За пределами королевства Она связана между Ликвидусом и Солидусом (т., Einti, t \ QP и др.)、 Ля’ Соответствует равновесному комплексу жидкой фазы и соответствующей твердой фазы. Области emnf, MNQH и gabh соответствуют наличию гетерогенных смесей твердых веществ Дыхательная фаза.
Смотрите также:
| Представление о зонной теории. Металлы, полупроводники, изоляторы | Твердые растворы |
| Основы физико-химического анализа | Соединения постоянного и переменного состава. Дальтониды и бертоллиды |
