Оглавление:






Тройные системы
- Тройная система g рисунок 13.8.Плавающий график Как впервые указал Гвербс, рыхлый раствор, содержащий 3 компонента (p = const. Состав раствора、 Точка равностороннего треугольника, где вершины a, b l C uoot * соответствуют 3 чистым компонентам.
Это не совсем верно, потому что каждая точка на фазовой диаграмме соответствует состоянию физически четко определенной системы, независимо от того, находится она на этой кривой или нет. По этой же причине нереально рассматривать фазовую диаграмму с диаграммой слияния как особую конфигурацию. Н. С. характеристические кривые в духе khulnakov. Do не поддаются исследованию термодинамическими методами. (Отредактированный))
Если взять стороны треугольника 1 такую диаграмму состояния часто называют кривой зависимости температуры кипения (или давления пара)от состава. Людмила Фирмаль
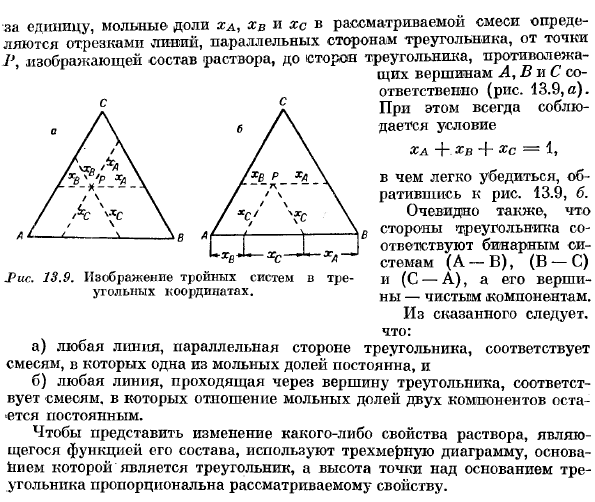
Существует обширная литература по 2-тернарной системе. Особо следует отметить, что N. W. D. Roozeboom работает. Умереть Heterogenen Gleicbgewichto (Амстердам 1901-1911), затем Schreinemakers и Фогель [50]. См. также работы Финдли и Бэнкрофта. Вода G. Это отличное приложение. Система терна РО (Лейпциг, 1933).Инженерный трансформатор, Б. А. Роджерс (Лондон, 1944). На единицу молярная доля xA, xb и xc в рассматриваемой смеси определяется отрезком, параллельным стороне треугольника, от точки 1, представляющей состав раствора, до стороны противоположного треугольника в вершинах A, Z? Каждое С(рис. 13.9, а). D£всегда в этом случае 0 / \ b / \условие задано / / \ Chl Xji Xs = 1 / gr’R / * v_p_ * a \легко увидеть、 / — \/\13.9 b, который будет цифрой. / kXc / xc / / Njrc \также、 L / / \ \ A / / \ \ D сторона треугольника [Дж! j-двоичный si- Тотем (A-B), (B-C) 1> Реф. 13.9. 3 и 3-компонентные изображения (C-A) и их вершины Координаты угля. очистите компонент с нами .
Из вышесказанного вы можете увидеть следующее: а) линия, параллельная сторонам треугольника, соответствует смеси, где 1 молярная доля является постоянной. Б) линия, проходящая через вершину треугольника, соответствует смеси, в которой соотношение молярной доли 2 компонентов остается постоянным. Трехмерная диаграмма используется для представления изменения свойств решения, которое является функцией конфигурации.
- Его основание-треугольник, и высота точки над основанием треугольника пропорциональна рассматриваемому свойству. Тройная система коагуляции Рассмотрим растворы 1 и 3 компонентов А, В и С, которые не взаимодействуют химически друг с другом и находятся в равновесии с одним из твердых компонентов. Тогда c = H, f = 0,0 = 2, оттуда w = 3, система трехвариантна. Принимая давление и состав раствора (p, Chl, m <>в качестве независимых переменных), можно отслеживать, как изменяется равновесная температура при изменении переменных.
При постоянном давлении на рис. 13.10 (1) твердая фаза показана в зависимости от состава (chl, xb).Поверхность Б Минск-ИКК \является равновесной поверхности раствор-Кристалл компонента B, и c поверхности’k2kkya соответствует раствор-Кристалл с. Система творческих-Хрустальный л. Кривой Донецк \ B ’- это коагуляция кривой двойной наркотиков системы, которая образует эвтектику, а кривая B’fac с’С’ къА ’ относятся к BC и CA систем, соответственно. Линия Kk \соответствует трехфазной системе раствор-твердый компонент A-твердый компонент B. такая система、 Так… C’ / год / И затем Рис. 10/13.Эвтектический Тип 3-компонентная жидкость-твердая равновесная поверхность системы (p = const). Определенное давление, точка, обозначающая состав раствора, находится на одной линии. 3 линии kiK, K » 2K и k $ K пересекаются в точке K, которая является тройной эвтектикой point. In в связи с этим существует 4 равновесия (время: жидкие и твердые компоненты А, В и с).Эта система представляет собой единую антенну, но при постоянном давлении только 1 точка соответствует этому состоянию.
То есть точка зрения К. Воздействие воздуха Как и прежде, результаты экспериментов, выполненных при постоянном давлении в присутствии воздуха, могут легко показать, что воздух может быть выражен таким же образом, как и в отсутствие it. In фактически, воздух можно считать новым компонентом, но изменчивость системы не меняется, потому что появляется и новая фаза (пар). Перемещение точки Диаграмма Kk\, Kk% и Kkz (см. Рисунок 13.10) проецируются на нижнюю часть диаграммы, в результате чего получается треугольная фигура, показанная на рисунке. 11/13.Рассмотрим, что происходит, когда раствор остывает
Сначала это было при температуре точки плавления. Когда перпендикуляры, падающие из точки P, сначала кристаллизуются на поверхности B’K \ Kkj \ компонента B, начинается затвердевание, в результате которого происходит концентрация A и C в растворе increases. In в этом случае соотношение концентраций А и с остается постоянным, поэтому состав раствора изменяется вдоль линии РР, начиная с точки B. As как только он достигает точки P1, начинается кристаллизация компонента C, а по мере снижения температуры изменяется состав III жидкой фазы (PuSt 1311 3a1).、
Квантование всех 3-х компонентов при эвтектическом соотношении, какой бы ни была начальная конфигурация системы, завершается при полном отверждении системы, достигает эвтектической точки при достаточном охлаждении. В качестве примера троичной системы, работающей описанным способом, можно назвать систему Bi-Ph-Sn. Би: / ПЛ. = 268°с; рН: Т ЛП. = 325°с; зп: Т ЛП. = 232°с Bi-PI) двойная эвтектика (55 мас.%ЗП): 127°С; PB-Sn двойная эвтектика (63 мас.%ЗП): 182°С; Bi-Sn двойная эвтектика v (58 мас.%Би): 133°С; Bi-PI) — тройная эвтектика Sn (52 мас.%Висмут; 32 МАС.%рН; 16. рт.%ЗП):96°С Если компоненты системы могут образовывать твердое решение, вы, естественно, получите более сложную диаграмму.
An примером такой системы является система, содержащая карбонат кальция, оксид кальция и диоксид углерода. Эти вещества взаимодействуют по реакции. СаСО3 ^ САО + СО2. Поскольку система имеет 3 фазы, c = 3, r * = 1, и система имеет только 1 степень свободы. Система представляет собой единый вариант, и в состоянии равновесия ее состояние полностью определяется установлением temperature. So например, следующее равновесное давление углекислого газа соответствует различным температурам. ° C мм рт. ст. 725 71,2 7G) 0 100 815 230. 860 420
Тройная система, в которой 3 компонента связаны химическими реакциями 1. изменчивость такой системы снижается, в результате чего ее функционирование становится. Людмила Фирмаль
Смотрите также:
| Однокомпонентные системы | Термодинамическое состояние |
| Двойные системы. Кривые плавления. Эвтектические точки. | Идеальный газ |
