| 🎓 Заказ №: 22215 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Дайте обоснованный ответ, в каком направлении может самопроизвольно протекать заданная реакция? Составьте схему гальванического элемента, в котором протекает эта реакция. Напишите уравнения анодного и катодного процессов, а также суммарное ионно-молекулярное уравнение. Определите ЭДС при концентрациях потенциалообразующих ионов в анодном и катодном пространстве, равных 1 л моль .
Решение Окислительно-восстановительная реакция может протекать в прямом направлении в том случае, если электродный потенциал окислительной системы больше потенциала восстановительной системы. Стандартный электродный потенциал – это электродный потенциал, измеренный при стандартный условиях (Т = 298 K; концентрация потенциалопределяющих ионов [Mеn+] = 1 моль/л, давление P = 101,3 кПа) относительно стандартного водородного электрода. Стандартные электродные потенциалы двух имеющихся систем имеют следующие значения Cu e Cu 2 2 E B Cu Cu 0,34 / 2 Ni e Ni 2 2 E B Ni Ni 0,25 / 2 Первая система является окислительной, вторая восстановительной. Таким образом, медь является катодом, никель – анодом. Схема гальванического элемента
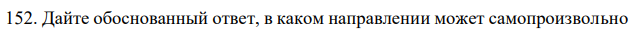

| Научись сам решать задачи изучив химию на этой странице: |
| Услуги: |
Готовые задачи по химии которые сегодня купили:
- Рассчитайте количество карбоната натрия, необходимое для приготовления 500 мл 0,2 н раствора.
- Некоторое количество металла, молярная масса эквивалентов которого равна 28 г/моль, вытесняет из кислоты 0,7 дм3 водорода, измеренного при нормальных условиях.
- Чем можно объяснить большую восстановительную способность щелочных металлов. При сплавлении гидроксида натрия с металлическим натрием последние восстанавливает водород щелочи в гидрид-ион.
- Рассчитайте навеску перманганата калия, необходимую для приготовления 500 мл 0,05 н раствора.
- Напишите электронные формулы атомов элементов с порядковыми номерами 9 и 28.
- Сколько граммов и моль оксида меди (II) образуется при окислении 4 г меди?
- Структура валентного электронного слоя атома элемента выражается формулой: а) 4s24p3 ; б) 4s24d4 .
- Для данных реагентов (даётся реакция нейтрализации): Zn(OH)2 + HNO3.
- Данных реагентов (даётся реакция гидролиза соли): FeCl2 .
- Какую ковалентную связь называют -связью и какую -связью?
