Оглавление:




О ионной связи
- Об ионных связях. Первоначально опубликовано как kossel A916 Разнородные атомы стремятся приобрести конфигурацию внешней Ее благородная газовая оболочка. Это достигается за счет отдачи и монтажа. Электроны обусловлены нейтральными атомами химических элементов. Отдавая атомы Электроны преобразуются в положительно заряженные ионы (катионы).
- Атом Присоединение электронов превращается в отрицательно заряженный ион (Анион.) Вот в чем суть Теория ионной связи. Согласно теории ионных связей, в решетке ионных кристаллов(например、 NaCl) не только вызывает притяжение между противоположными ионами、 Отталкивание одноименного Иона.
Химическая связь обусловлена статическим электричеством Тяга образовала противоположные ионы. Людмила Фирмаль
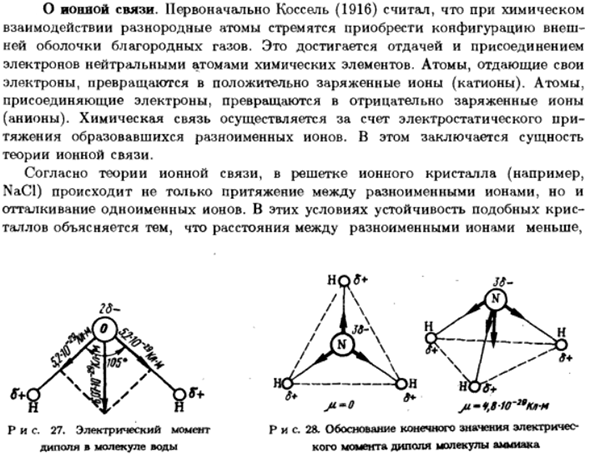
В этих условиях устойчивость таких Талова объясняется тем, что расстояние между противоположными ионами невелико Тридцать шесть- 27.Электрические моменты Диполи молекул воды P и s. 28.Обоснование конечной стоимости электроэнергии Дипольный момент молекулы аммиака Больше между тем же именем. Поэтому гравитационное притяжение кулона будет преобладать Он обеспечивает ионную связь с силой отталкивания. Однако в идеале не было бы никаких ионных соединений вообще、 Истинная ионная связь тоже.
Даже с химическими взаимодействиями, большинств Положительные и отрицательные элементы образуют соединения Химическая связь не является 100%ионной. Таким образом, молекула и В кристалле ионная связь、 Ионная связь. Во-первых, экспериментальные доказательства этого Данные об эффективном заряде атомов, входящих в состав соединения. Эффективный заряд атома, входящего в состав соединения, определяется как Алгебраическая сумма отрицательных и положительных зарядов Ядерный заряд.
В настоящее время известно более десятка экспериментальных методов. В большинстве случаев определение эффективных сборов @ , 1-0. 3) E, эти обязанности сбалансированы с точностью для того чтобы высчитать Квантовая химия и твердое тело theory. In стол. 9 показывает данные выше Активный атомный заряд, полученный методом рентгеновской спектроскопии Много типичных неорганических веществ. Знак «+ » включен Заряд металлических элементов, знак » — » — электроотрицательность Атомы.
Только чистые щелочные галогениды близки к чистым ионным соединениям. Высокий, но для них эффективная плата не достигла единства. Все остальное Соединения, содержащие галогениды, оксиды, сульфиды кальция и магния、 Только частично ионный. В дальнейшем、 Электроотрицательные атомы (кислород, сера) редко превышают 1. С другой стороны, заряд металлических элементов (кальция, алюминия) Очевидно, не один.
Это означает, что энергия, которая связывает 2 От электронов к кислороду и сере (сродство для электронов 2-го порядка), отрицательный Teruya. By вычисление, сродство для вторичных электронов является Кислород составляет −732, а для серы-334 кДж / моль. Следовательно, тип Иона O2″, S2 ″ не существует*и все оксиды, сульфиды, независимо от активности Металлы не являются ионными соединениями. Когда действуют дважды заряженные ионы Многозарядные моноатомные атомы как волатильность нереальны, если их нет Отрицательный ион.
- Самопроизвольный переход электронов от атома металла к атому Тара почти не настоящая. Факты, потенциал Первичная ионизация даже для самых активных щелочных металлов Электронное сродство типичного электроотрицательного элемента выше. И С этой точки зрения, образование ионов Молекулы NaCl из элементов, начиная с первого потенциала ионизации натрия Равен 5,14 В, а сродство к электронам атома хлора составляет 3,7 эВ(ионизация Потенциал, выраженный в вольтах, численно равен энергии ионизации электрона Болт.)
Из квантовой механики, полное разделение зарядов Появление идеальной ионной связи A1 + B1 — никогда не может быть реализовано. Поэтому, вопреки довольно распространенному мнению о чистых ионах Соединения с полными ионными связями * * * на самом деле не существуют***.Между. Тем не менее, общепризнано, что большинство химических связей не имеют Органические соединения обладают ионными свойствами. Это объясняется в 2 источниках.
Из-за волновых характеристик электрона, вероятность близка к этому электрону Ядро атома а может быть маленьким, но оно не равно нулю. Людмила Фирмаль
Причина достаточно распространенная. Во-первых, почти все химические реакции Он был изучен в водной среде и выражен по существу ионно reactions. In В то же время, поведение веществ в водных растворах радикально отличается Из характеристик при отсутствии water. So, соляная кислота Самые сильные электролиты: хлористый водород, растворенный в воде, полностью растворяется Он связывается с ионами водорода и хлора.
В основном благодаря этому факту, это было возможно HC1 обеспечивает ионное связывание молекул. Однако хлористый водород безводный Это почти неионное соединение с эффективным зарядом. Водород и хлор равны+0,17 и −0,17 соответственно. Во-вторых, в свете учения Об ионных связях в неорганической химии Фактическая отрицательная валентность (электрическая валентность).Даже если это невозможно.
Где отдача и сцепление электронов часто является валентностью электронов Нос, то есть ионные связи. Это неорганическое вещество Очень важную роль играет электронная теория окислительно-восстановительных процессов Реакция образования предполагающая переход электронов от восстановителя Чтобы oxidants. In в этом случае состояние окисления было полностью идентифицировано как: Полезно рассчитать количество ковалентных связей и дать их соединение.
Среди электронов, по-видимому, неионными соединениями считались вещества с ионами Никакая связь. С другой стороны, понятие окислительных состояний не имеет общих черт. * Согласно экспериментальным данным по рассеянию молекулярных Пучков, эти ионы являются Он действует как сильно неустойчивая частица с жизнью около 10 секунд. * * Как ионы характеризуются дискретными зарядами целых чисел Тупые, например, A1+, A2+, A3+, B1″, B2 ″ и т. д. * * *
Такие соединения в основном называют ионными. Ни эффективного атомного заряда, ни действительного количества связей Образует указанный атом (валентность). Поэтому необходимо обсудить степень ионизации (Степень ионности).Кроме того, чем выше степень ионности связи 、 Эффективный заряд атомов, составляющих соединение. «ФВ- «Эффективный заряд» терпит неудачу, потому что он фактически вычисляется как экспериментальный. Их значение-это фактический заряд атомов в соединении. Идеальный газ и идеальное решение плюс идеальная ионная связь Рами-типичный пример научной абстракции.
Смотрите также:
| Длина химической связи | Ковалентная связь |
| Электрический момент диполя и направленность связи | Понятие о квантовой химии |
