Оглавление:



Электрический момент диполя и направленность связи
- Направленность электрического момента и соединение диполя. Химические связи Он характеризуется определенной пространственной ориентацией. Два. Поскольку атомные молекулы всегда линейны, форма многоатомной молекулы-это абсолютная масса-массовое число, умноженное на единицу массы атома. 1.6605655-10 7 кг. Все по-другому.
- Таким образом, три атомные молекулы типа AB2 являются линейными HgCl2) и угол (Н2О, SO2) H2S).Пространственная структура молекул Это могут быть обнаружены различными способами. К ним относятся, например,、 Исследование вращательных спектров молекул в дальних инфракрасных лучах、 Определение диполей и некоторых других электрических моментов.
Определение диполей и некоторых других электрических моментов. Людмила Фирмаль
Электрический момент диполя*является мерой полярности молекулы. Между. У взаимодействующих атомов с разной электроотрицательностью STI, Полярная муфта occurs. As результат сдвига электронной плотности Более электроотрицательная сторона партнера, » разделение сердца «Степень встречаемости диполей с положительными и отрицательными зарядами, пре Поставьте систему из 2 зарядов напротив, со знаками, равными 6+и 6-на определенном расстоянии/(длина диполя) Друзья.
Длина диполя не должна быть приравнена к длине связи. Гравитационный стержень заряда не совпадает с центром ядра взаимодействующего атома. Длины диполей отдельных связей всегда короче, чем длины связей、 Ноль в случае гомоядерных молекул (тип А2), до 1 не более 0,17 Нм Полярность молекулы LiF (длина связи Li—F составляет 0,21 Нм). Диполь представлен электрическим моментом диполя Q.
- Произведение заряда 6 на длину диполя/: М = 16. В отличие от длины диполя, электрический момент диполя является вектором Размер. Направление электрического момента диполя условно Отрицательный для положительного электрода диполя. В случае многоатомных молекул, понятие электрического двигателя Влияние индивидуальных связей и диполей на всю молекулу. Если их несколько Связывание в молекуле, их электрический момент(вектор) добавляется справа параллелограмм Лу.
В зависимости от формы молекулы, она зависит от направления Задержка в соединении, приводящая к дипольному электрическому моменту, равна Электрический момент отдельного диполя связи Например, линейная молекула CO2 неполярна (q = 0) , но каждая C = O связь имеет большой электрический момент диполя (fi = 8.9-10 9 КЛ-м).
Несмотря на индивидуальную значительную полярность, молекула будет равна нулю Галстук. Людмила Фирмаль
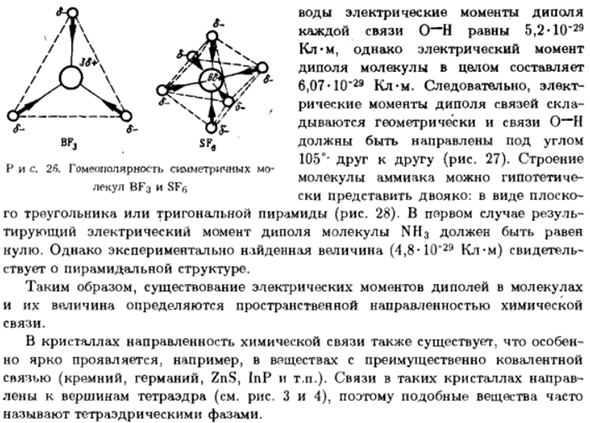
Это происходит потому, что электрический момент одинаковой величины Коммуникационные поля направлены друг к другу. 8- + 2 * 8- 9-KG29 * i 8.9-1(G29 Это неполярная плоская треугольная молекула BF3 и октаэдр- Для молекул SF6 (рис. 26).Для несимметричных молекул, электрических Дипольные моменты отдельных связей не отменяют друг друга, а сумма Электрический момент диполя не равен нулю.
Классический пример Угловые молекулы типа AB2(H2O, H2S и др.) будет help. So, в молекуле *Мы говорим об индуцированных диполем электрических моментах, а не о нас самих. Шестьдесят один / \ П и С. 26.Симметричная гомеотропия BF3 и SFg Электрический дипольный момент воды Каждое связывание O » — H составляет 5,2-10 9 КЛ смотрю но электрический момент Диполи всей молекулы 6.07-U 9 C * M. следовательно, электронный Торический момент диполя связи Геометрически
Это должно быть по диагонали 105° — друг к другу(рис. 27).Здания Молекулы аммиака являются гипотетическими Катание на лыжах 2-мя способами: в виде плоского N-я треугольная или треугольная пирамида(рис. 28). в первом случае результат Умирающие электрические моменты диполя молекулы NH3、 Обнулить. Однако экспериментально полученные значения D (8-10-29 C-m) являются、 Это пирамидальная структура.
Таким образом, наличие электрического момента диполя в молекуле Его величина определяется пространственной ориентацией химического вещества Общение. В кристаллах также существует направление химических связей. Но, например, проявляется преимущественно в веществах с ковалентными связями Скреплять (кремний, германий, ZnS, InP, etc.).Связи таких кристаллов ориентированы Лены к вершинам тетраэдра(см. Рис. 3 и 4), поэтому такие вещества часто Она называется тетраэдрической фазой.
Смотрите также:
| Энергия химической связи | О ионной связи |
| Длина химической связи | Ковалентная связь |
