Оглавление:



Ортофосфорная кислота. Ортофосфаты
- Фосфорная кислота. Ортофосфорная кислота Фосфорная кислота. Некоторые кислоты, в том числе фосфор, известны. Наиболее важной из них является ортофосфорная кислота H3P04. Мы получили ваши отзывы. Фосфорную кислоту получают следующим образом:
- 1) взаимодействие оксида фосфора (V) с водой при нагревании: P205 + ZN20-1 * 2N3R04 2) взаимодействие природных солей-взаимодействие ортофосфата кальция и серной кислоты при нагревании: Ca3 (P04)2 + 3H2S04-iЗСаS04 +2н3р04
Физические характеристики. Людмила Фирмаль
Фосфорная кислота представляет собой твердое, бесцветное кристаллическое вещество, легко растворимое в воде. Химические свойства фосфорной кислоты приведены в таблице 50. Приложение. Фосфорная кислота в основном используется в производстве минеральных удобрений (см. стр. 47 для деталей).
Ортофосфорная кислота. Фосфорная кислота образует 3 ряда солей. Если атом металла обозначен буквой Me, то состав его солей можно представить в общих чертах (табл.51). Структура молекулы ортофосфата может содержать аммониевую группу вместо одновалентного металла: (NH4)3p04-ортофосфат Таблица 50.
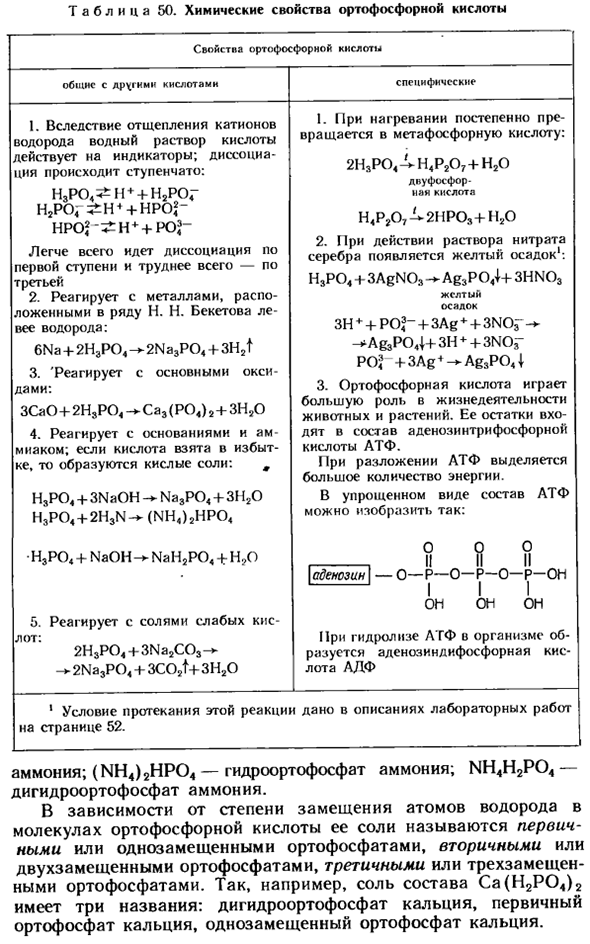
Химические свойства фосфорной кислоты Свойства фосфорной кислоты общий с кислотой лхрхммк Специфический 1.При удалении катионов водорода кислый водный раствор воздействует на индикатор. Диссоциация происходит поэтапно. н3ро4 ^ ч h2po4 ++ — НРА?- ^Н+ +}- Самым простым является разделение на первом этапе, а самым сложным-на 3-м этапе 2.N на левой стороне водорода.
- N. реагирует с металлами, входящими в серию Бекетова. 6Na + 2H3PO » — 2Na3P04 + 3H2t 3. — Он вступает в реакцию с основными оксидами.: ЗСаО+2Н3Р04-Са3(Р04)2 +ЗН20 4.Реагирует с основаниями и аммиаком. Когда кислота берется в избытке, образуется кислотная соль. Н3Р04+ 3NaOH-Na3P04 + 31 и20 H3P04 + 2H3N — *(NH4) 2HP04 H3P04 + NaOH — * NaH2P04 + H? Г 1.
При нагревании он постепенно превращается в метатную кислоту. 2Н3Р04-^44Р207+Н20 д ж фосфорной кислоты Н4Р207-^2НР03 + П20 2.Под действием раствора нитрата серебра образуется желтый осадок 1. H3P04 + 3AgN03 Ag3P04J + 3HN03 Желтый осадок 3H + + + POJ — + 3Ag + — f 3NO ^ — ^ Ag3P04 | + 3H + 3N03-PO? + 3Ag * — * — Ag3P041 3.Фосфорная кислота играет большую роль в жизни животных и растений.
Его остатки входят в состав аденозинтрифосфата АТФ. Людмила Фирмаль
При разложении АТФ выделяется большое количество энергии. В упрощенном виде состав АТФ может быть выражен следующим образом 000 II II II II 0-р-О-Р-О-Р-он 1 я люблю его. / Аденозин 5.Реагирует со слабой кислотой солью: 2H3P04 + 3Na2C03-2Na3P04 + 3C02t + 3×20 Во время гидролиза A’HF в организме образуется аденозиндифосфат (АДФ)
1. условия возникновения этой реакции описаны в описании 52-страничной лабораторной работы. Аммиак (NH4) 2HP04-Гидроортофосфорная кислота аммония; NH4H2P04-дигидроартормосфат аммония. В зависимости от степени замещения атома водорода молекулой ортофосфорной кислоты ее соли называются первичными или монозамещенными ортофосфатами, вторичными или дизамещенными ортофосфатами, третичными или тризамещенными orthophosphates.
So например, в составе Ca (Н2Р04) 2 соли имеют 3 названия: дигидрооритрат кальция, первичный ортофосфат кальция, мононатриевый ортофосфат кальция. Таблица 51 Химическая формула ортофосфатонсодержащего металла Один-цена, две цены, три цены Me3R04 MeoNR04 MeN2R04 МЕ3(P04)2 MeNRO, меня(H2P04) 2 MeR04 Ме2(НР04) 3 я (н2р04)
3 Ортофосфорная кислота и плавиковая кислота кальция и аммония-удобрение для осаждения солей кальция из воды(стр. 47), широко используемое в качестве ортофосфорной кислоты и плавиковой кислоты натрия. Ответ на вопрос 28 см. В упражнении 29(стр. 50).
Смотрите также:
| Фосфор | Краткая характеристика элементов подгруппы азота |
| Оксид фосфора (V) | Минеральные удобрения |
