Оглавление:


Процесс образования растворов
- Процесс образования раствора. Обычно произносится при растворении Термический эффект (эндотермический или экзотермический), изменение объема (объем- Общий объем раствора не равен общему объему компонента) Например, когда наблюдается растворение гидроксида калия в воде Мощный нагрев раствора: Ко + Ак = ко-Ак(к = −54 кДж)、
- При растворении аммиачной селитры-охлаждение: Водный раствор NH4NO3 += NH4NO3-aq (AN = +25 кДж). При смешивании 100 мл воды с эквивалентным количеством этилового спирта, не ожидаемое количество С раствором в 200 мл можно получить только около 180 ml. As в результате Ния, объем dropped. Имеет цвет с сильным голубым возникновением. Все эти явления указывают на изменение химических свойств компонентов В процессе своего становления тов solution.
It это не сульфат меди безводный. Людмила Фирмаль
In в связи с этим Д. И. Менделеев.、 Сторонники современной теории решений в 1887 г.、 Химические аспекты образования раствора: «Раствор-это жидкость Диссоциационная система, образованная частицами растворителя, растворяется Вещества и их специфические нестабильные, но экзотермические соединения、 Происходит между ними, в зависимости от характера Элементы начала.«
Основное содержание современной химической теории Решение отражено в этом определении, но оно необходимо с точки зрения новых данных Уточните, что промежуточные соединения не могут быть определены Соединения постоянного состава. Промежуточные соединения, образующиеся в межмолекулярных растворах Растворители и частицы растворенных веществ (молекулы, ионы, атомы) Он называется сольват.
- Для водных растворов такими соединениями являются Гидрат. Иногда гидрат высвобождается, потому что он очень сильный и Растворенное вещество из раствора воды входит в состав растущих crystals. In Химически связанная форма. Такие кристаллы называются кристаллогидратами、 Образующая их вода кристаллизуется. Примеры кристаллогидратов Большое количество: CuSO4 * 5H2O, Na2SO4 * 10H2O, CrC13 ′ 6H2O, etc.
Сохраняет цветовые характеристики каждого раствора. Служить Доказательство существования в растворе аналогичного аквакомплекса. С термодинамической точки зрения растворение всегда сопровождается Энергия Гиббса declined. . -Понятия не имею..- ¦- ’147 О Сто восемьдесят ИСО Программное обеспечение Мне 120. Мне 100 лет. Мне 80. Мне 60. К ? 7/7 Температура, С Рисунок 78.
In сложение, независимо от признаков изменения энтальпии; Людмила Фирмаль
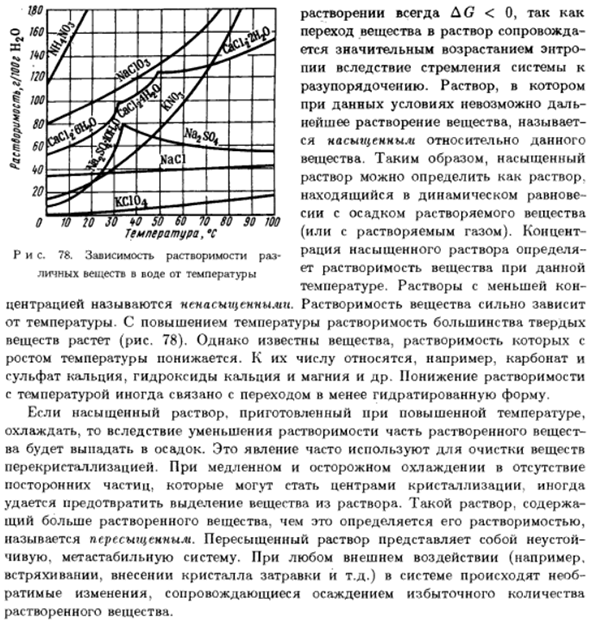
Зависимость растворимости Отдельные вещества в воде от температуры / И затем Дж Один ! Вы «футовый ? 5л —¦ НАК. В х / 「 7 секунд Один * » ¦ —¦ Всегда AG <0 Переход вещества в раствор Это значительное увеличение ПИИ в соответствии с требованиями системы Необузданный. Решение В этих условиях невозможно Небольшое растворение вещества называется Насыщает в этом плане Вещество.
Насыщение Решение может быть определено как решение. В динамическом равновесии К ним относятся растворимые осадки (Или используйте растворимый газ).Сосредоточенность Определяется радио насыщенного раствора Растворимость некоторых веществ Температура. Меньше Кон-решений Центрирование называется ненасыщением. Растворимость вещества очень зависит. От температуры.
Когда температура повышается, растворимость большинства твердых веществ Растущее вещество(рисунок 78).Но вещество с его растворимостью известно Повышение температуры. К ним относятся, например, карбонат и Сульфат кальция, гидроксид кальция, гидроксид магния и др. Пониженная растворимость Температура может быть связана с переходом в менее водянистую форму. Когда насыщенный раствор готовится при высокой температуре、
Часть растворенного вещества охлаждается и растворимость уменьшается Сумма выпадает в осадок. Это явление часто используется при очистке веществ. Recrystallization. In отсутствие медленного и нежного охлаждения Посторонние вещества, которые могут стать центром кристаллизации, иногда Можно предотвратить выделение веществ из раствора.
В том числе и такие решения Растворимый, чем определяется его растворимость、 Его называют перенасыщенным. Пересыщенный раствор нестабилен. Чистый и метастабильный system. In случай внешнего воздействия(пример: Встряхивание в системе, создание кристаллического семени и т. д.) Повторяющиеся изменения с избыточным количеством осадков Растворенное вещество.
Смотрите также:
| Жидкое состояние. Структура жидкости | Идеальный раствор. Законы разбавленных растворов |
| Дисперсные системы. Растворы | Электролитическая ионизация. Степень и константа ионизации |
