Оглавление:


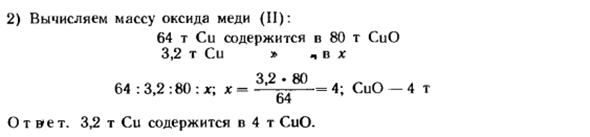

Расчеты по химическим формулам
- Расчет по химической формуле 1.Найти массовое соотношение между элементами по химической формуле сложных веществ. Проблема. Найдите массовое соотношение между элементами гидроксида кальция. Решение. 1) Найти молярную массу гидроксида кальция: M (Ca (OH))=> 40 4-(16 + 1)•2 = 74; M = 74 г / моль
- 2) найти массовое соотношение кальция, кислорода и водорода: Ca: O: H= 40:32:2-20:16:1 Ответ. Соотношение масс между элементами 20: 16: 1 2.Найти содержание элементов в массовой доле и процентное содержание сложных веществ. Проблема. Рассчитайте содержание элемента как по массовой доле, так и по соотношению гидроксида натрия.
Решение. 1) Найти молярную массу гидроксида натрия: M (NaOH)= 23 + 16 + 1 = 40; м-40 г / моль Людмила Фирмаль
2) рассчитайте массовую долю натрия. 5/40. д. Раствора NaOH включает 5/23. d. Na 1 «> NaOH » x、 40:1-23:、; −1 * 23-0.575; На-5 Марта 0. 575 д. или 57,5%40 Из этого становится ясно, что для нахождения массовой доли элемента необходимо разделить его массу на молярную массу вещества. Двадцать три — =0,575; Na — 5 месяц 0,575 д. или 57,5%4U 3) вычислить массовую долю кислорода: — ^- =0,4, может быть 0-0. 4. д. или 40.%
4) вычислить массовую долю водорода: — L = 0,025, H-0,025 5 мес. d. или 2,5% 40 」 5) Проверьте правильность расчетов. 0.575 + 0.4 + 0.025-1.00 (5 мая Д. Мне очень жаль. 57.5 + 40 + 2.5 = 100(%) Ответ. NaOH содержит 5 месяцев 0,575. d. NA, или 57,5%, снизившись на 0,4 процентных пункта с 5 апреля. d. или 40%, O и 0.025 5 месяцев. д.. Или 2,5%. Н. Примечание содержание водорода также может быть рассчитано по разнице. 0,575 + 0,4 = 0,975 (5 месяцев d.) 1,0-0,975 = 0,025(5 месяцев d.)57.5 + 40 = 97.5(%)100-97.5-2.5(в%).
- 3.Найти массу элемента в пределах определенной массы сложного вещества. Проблема. Рассчитайте количество алюминия, содержащего 408 тонн оксида алюминия. Решение. 1) Найти молярную массу оксида алюминия: M (A12Oe)-27•2 + 16•3-102; M (A1203) −102 г / моль
2) рассчитайте массу алюминия 1, содержащегося в 408 тоннах оксида алюминия. 102-тонный A203 содержит 54-тонный AI и 408-тонный A12Oe » x 102. 408-54:*; x-12 ^^ 1 = 216; A1-216t. 408-тонный A12Oe содержит 216 тонн AI. Если указаны примеси, то сначала рассчитывается масса чистого вещества, содержащегося в смеси. Затем выполните описанные выше действия.
4.Найти массу комплексного вещества относительно удельной массы элемента. Людмила Фирмаль
Проблема. Содержит ли оксид меди (II) 3,2 тонны меди? Решение. 1) молярная масса оксида меди (II): M (CuO) −64 + 16 = 80; UI (CuO)= 80 г /моль 1 далее расчет производится в единицах массы, указанных в задаче. 2) вычислить массу оксида меди (I): 64 Т Cu входит в состав 80 т CuO 3.2 Т Cu> * n x 64:3,2: 80:*; х-3.2 * 80-4; Куо-4Т 64 Ответ. 3.2 t Cu входит в состав 4 t CuO.
Смотрите также:
| Краткая характеристика элементов подгруппы кислорода | Расчеты по уравнениям химических реакций |
| Вывод химических формул | Расчеты с использованием понятия «моль» |
Если вам потребуется заказать решение по химии вы всегда можете написать мне в whatsapp.
