Оглавление:


Электроотрицательность химических элементов
- Химия электроотрицательность Элементы С точки зрения теории строения атомов, отнесение элементов к металлам и неметаллам определяется способностью их атомов отдавать или объединять электроны.
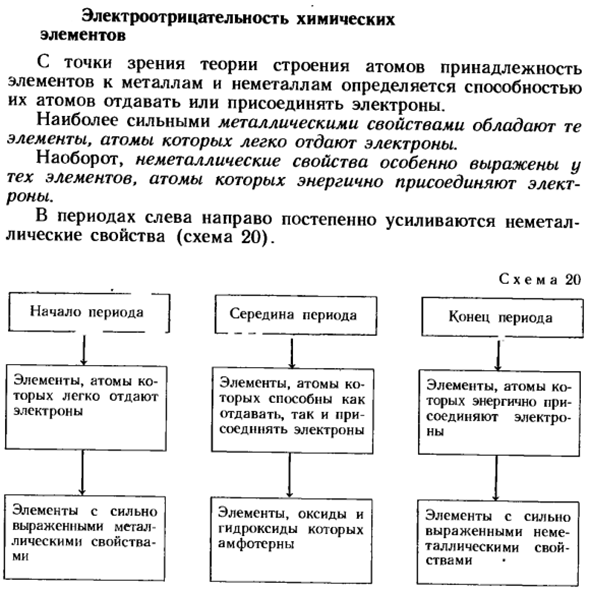
- Наиболее мощными свойствами металлов обладают элементы, в которых атомы легко высвобождают электроны. Напротив, неметаллические свойства особенно выражены в элементах, в которых атом энергетически объединяет электроны. В период слева направо неметаллические свойства постепенно увеличиваются(схема 20). Схема 20
Природа атома, притягивающего к себе электроны, называется электроотрицательностью 1. Людмила Фирмаль
Понятие электроотрицательности в дальнейшем помогает понять свойства свойств химических связей. Абсолютное значение электроотрицательности выражается в числах, которые мешают практическому применению. Поэтому электроотрицательность лития обычно считается единицей. Рассчитана электроотрицательность других элементов accordingly.
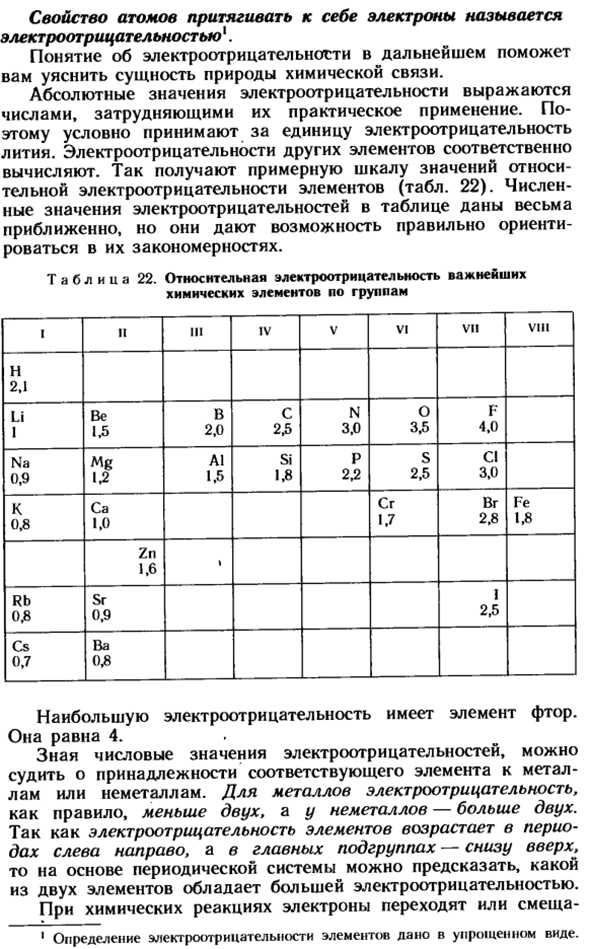
So, получаем приближенную шкалу относительного значения электроотрицательности элемента (табл. 22).Численные значения электроотрицательности в таблице приведены очень приблизительно, но они позволяют нам правильно ориентироваться в законах. Таблица 22.
- Относительная электроотрицательность наиболее важных химических элементов в группе 1 II III IV V VI VI VI VII VIII П 2.1 Ли 1 Быть В 1.5 2.0 2.5 3.0 3.5 4.0 С Н О Ф На 0,9 мг А1 1.2 1.5 1.8 2.2 2.5 3.0 Си П С ки К Ка-0.8 1.0 1.7 КР Бр 2.8 1.8 Фе ЗН 1.6 я 0.8 0.9 Ср РБ Я 2.5 В CS 0.7 Ба 0.8 Наибольшая электроотрицательность имеет элемент фтор. Равно 4.
Если известна численная электроотрицательность, то можно определить принадлежность соответствующих элементов к металлам или неметаллам. Поскольку электроотрицательность элементов периодически возрастает слева направо и снизу вверх в основной подгруппе, то какой из 2-х элементов является более электроотрицательным, можно предсказать на основе периодической системы.
Для металлов, как правило, электроотрицательность меньше 2, а для неметаллов-больше 2. Людмила Фирмаль
В химической реакции электроны перемещаются или смещаются Определение электроотрицательности 1 элемента представлено в упрощенном виде. К атомам элемента с большей электроотрицательностью. Таким образом, информация об электроотрицательности элементов имеет особое значение при характеристике химических связей и валентности. Ответьте на вопрос I (стр. 134).
Смотрите также:
| Значение периодического закона | Основные типы химической связи |
| Жизнь и деятельность Д. И. Менделеева | Кристаллические решетки |
Если вам потребуется заказать решение по химии вы всегда можете написать мне в whatsapp.
